专利摘要
本发明公开了一种羧甲基化五味子多糖及其制备方法和应用,属于多糖改性技术领域。该羧甲基化五味子粗多糖的得率为88.37±1.65%,羧甲基化取代度为0.724±0.022,溶解度为0.5±0.04mg/mL,是原五味子多糖溶解度的5倍。羧甲基化五味子多糖的溶解度为12.5±0.26mg/mL,分子量为3.4×106Da,单糖组成为:甘露糖、葡萄糖和半乳糖,其摩尔比为1:44.84:3.71。本发明反应温度在40‑80°C、反应时间在1‑8h,氯乙酸终浓度在0.005‑0.08g/mL的条件下,所得羧甲基化五味子多糖的得率和取代度均较高,水溶性好,且对持久性有机污染物PCB126致小鼠免疫抑制有显著的改善作用,可提高小鼠脾脏和胸腺指数,增加血清中TNF‑α、IFN‑γ和IL‑2的水平,可作为免疫增强剂,用作功能食品和食品添加剂。
权利要求
1.一种羧甲基化五味子多糖,其特征在于:所述羧甲基化五味子多糖的分子量为1.698×104 Da,所述羧甲基化五味子多糖的单糖组成为:甘露糖、葡萄糖和半乳糖,摩尔比为1:44.84:3.71,所述羧甲基化五味子多糖的溶解度为12.24-12.76 mg/mL,所述羧甲基化五味子多糖在水溶液中呈聚集状形成分子链,所述分子链的厚度为0.1-1 nm。
2.权利要求1所述的羧甲基化五味子多糖的制备方法,其特征在于按照下述步骤进行:
(1)五味子粗多糖的制备:将新鲜五味子于55-65℃烘箱内干燥12-24h后进行粉碎,采用石油醚对干燥后的五味子进行回流脱脂2-3次,然后将脱脂后的五味子药渣以料液比1:10-1:15加入蒸馏水进行水提,取2-3次得到五味子多糖提取液,五味子多糖提取液经减压浓缩,采用80%的乙醇醇沉3-4次,得到的醇沉物经离心后,复溶、挥醇,经截留分子量为3000 Da的透析袋透析12-36h,真空干燥2-3h得到五味子粗多糖;
(2)五味子多糖的羧甲基化:将五味子粗多糖溶于异丙醇溶液中,机械搅拌使其充分溶解,五味子粗多糖和异丙醇料液比为1:30 - 1:40(g/mL),溶解温度为20-25℃,搅拌时间为15-20 min,搅拌速度为60-240 r/min,向溶解后的五味子多糖溶液中加入质量分数为15-20%的NaOH溶液进行碱化,NaOH溶液的加入量为异丙醇体积的20-30%,碱化温度为20-25℃,碱化时间为1-2 h,然后在搅拌状态下继续向碱化后的五味子粗多糖反应液中加入氯乙酸进行羧甲基化,氯乙酸加入量为0.005-0.08 g/mL,水浴温度为40-80℃,羧甲基化反应时间为1-8 h,待反应液冷却后调节反应液pH至中性,采用乙醇醇沉,离心后得到醇沉产物,将醇沉产物采用少量蒸馏水复溶后进行透析,透析结束后进行真空干燥得到羧甲基化五味子粗多糖;
(3)纯化:将步骤(2)得到的羧甲基化五味子粗多糖溶解于0.05-0.1mol/L 的NaCl溶液中,然后缓慢滴加至DEAE-52层析柱中,并采用0.05-0.2 mol/L的NaCl溶液进行梯度洗脱,绘制洗脱曲线,根据洗脱曲线分别收取合并洗脱液,得到羧甲基化五味子多糖不同组分,选取0.05mol/L NaCl的洗脱组分合并,经截留分子量为3000 Da的透析袋透析、真空干燥后,得到羧甲基化五味子多糖。
3.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(1)中五味子粗多糖的得率为15.9-19.8%,多糖含量为54.4-65.7%,溶解度为0.08-0.12 mg/mL。
4.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(2)中羧甲基化五味子粗多糖的得率为60.2-86.4%,羧甲基化取代度为0.41-0.71,溶解度为0.46-0.54 mg/mL。
5.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(1)中回流脱脂的温度为70-80℃,脱脂时间为1-2 h,水提温度为90-100℃,提取时间为4-6 h。
6.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(2)中采用80%乙醇醇沉24-48h,醇沉液以4000-5000rpm转速离心5-10 min。
7.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(2)中采用经截留分子量为3000 Da的透析袋透析首先采用流水透析,最后进行蒸馏水透析,流水透析时间为36-48h,蒸馏水透析时间为24-36h。
8.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(2)中真空干燥时间为2-3h,温度为20-25℃,真空度为-0.085 - -0.1Mpa。
9.根据权利要求2所述的羧甲基化五味子多糖的制备方法,其特征在于:所述步骤(3)中羧甲基化五味子粗多糖在NaCl溶液中经震荡加热溶解,震荡水浴的温度为50-60℃,震荡频率为120-160 次/分,震荡溶解的时间10-12h,然后对溶解后的溶液进行离心分离,溶液离心的转速为:4000-5000 r/min,离心时间为8-10 min;
所述步骤(3)中流水透析时间为36-48h,蒸馏水透析时间为24-36h,真空干燥时间为2-3h,真空干燥温度为20-25℃,真空干燥的真空度为-0.085 - -0.1MPa。
10.权利要求1所述羧甲基化五味子多糖的应用,其特征在于:所述羧甲基化五味子多糖能够作为免疫增强剂用于功能食品和食品添加剂中。
说明书
技术领域
本发明涉及一种羧甲基化五味子多糖及其制备方法和应用,属于多糖改性技术领域。
背景技术
五味子(Schisandra chinensis(Turcz.)Baill.)属木兰科五味子植物的成熟果实,主要的产于我国黑龙江、辽宁、内蒙古等地,是一种常见的滋补性中药,具有极高的药用和食用价值,已被列入可用于保健食品的物品名单(陆兔林,吴杨,季德黑.五味子多糖提取分离和药理作用研究进展.中国中药杂志,2014,39(4):751-754.)。研究发现五味子多糖作为五味子中主要的活性成分,其含量较高,并具有抗肿瘤、抗氧化、抗衰老、抗疲劳等多种生物活性(徐博,沈楠,赵丽晶.五味子各成分最新研究进展.中国老年保健医学,2013,11(5):74-74.),且对机体正常细胞和组织的毒性极小,具有较好的开发应用价值。
目前,多糖的结构修饰方法主要有磷酸酯化、羧甲基化、乙酰化等。羧甲基化修饰作为一种主要的化学修饰法,是指向多糖链上引入羧甲基,此种修饰方法对多糖的溶解度及电负性均有较重要的影响(江乐明,樊灿梅,聂少平.羧甲基化大粒车前子多糖的制备及其生物活性研究.食品科学,2013,34(22):10-14.)。研究发现,一种碱溶性银耳多糖,不溶于水,在通过羧甲基化修饰后,其在水中的溶解度提高至36.38mg/mL(吴琼.羧甲基化碱溶性银耳多糖的研究.长春大学学报:自然科学版,2009,19(10):66-68.)。2005年,郭祀远等申请的专利“羧甲基裂褶多糖制备方法及在化妆品和抗肿瘤药物中应用”(申请号:CN200510101678.X)中,利用氯乙酸、氢氧化钠等常规试剂对裂褶多糖进行羧甲基修饰,改善了其溶解性能并保持了其良好的流变性能和抗肿瘤活性。2011年,仰榴青等申请的专利“一种羧甲基化黑木耳多糖、粗多糖及其制备方法和应用”(申请号:CN201110219047.3)中,采用异丙醇法对黑木耳多糖进行羧甲基修饰,使其溶解度达到0.6mg/mL,是原糖溶解度的6倍,且其体外抗氧化能力也得到显著提高。
本发明人在五味子多糖的分离纯化、结构表征及抗肿瘤活性的前期研究中发现,五味子多糖的水溶性不理想,制约了其进一步的深入研究及开发应用。因此,本发明人对五味子多糖进行羧甲基化修饰,初步确定其结构特征,提供一种利用响应曲面法优化羧甲基化五味子多糖的工艺,并研究了该羧甲基化五味子多糖对持久性有机污染物PCB126所致的免疫毒性的干预作用。有关五味子多糖羧甲基化衍生物的制备及其工艺优化的研究至今未见国内外文献报道,也未见相应专利公开。
发明内容
本发明的目的是为了解决五味子多糖的水溶性不理想,制约了其进一步的深入研究及开发应用的缺点,提供了一种羧甲基化五味子多糖及其制备方法和应用。
本发明采用如下技术方案:一种羧甲基化五味子多糖,所述羧甲基化五味子多糖的分子量为1.698×104Da,所述羧甲基化五味子多糖的单糖组成为:甘露糖、葡萄糖和半乳糖,摩尔比为1:44.84:3.71,所述羧甲基化五味子多糖的溶解度为12.24-12.76mg/mL,所述羧甲基化五味子多糖在水溶液中呈聚集状形成分子链,所述分子链的厚度为0.1-1nm。
羧甲基化五味子多糖的制备方法,按照下述步骤进行:
(1)五味子粗多糖的制备:将新鲜五味子于55-65℃烘箱内干燥12-24h后进行粉碎,采用石油醚对干燥后的五味子进行回流脱脂2-3次,然后将脱脂后的五味子药渣以料液比1:10-1:15加入蒸馏水进行水提,提取2-3次得到五味子多糖提取液,五味子多糖提取液经减压浓缩,采用80%的乙醇醇沉3-4次,,得到的醇沉物经离心后,复溶、挥醇,经截留分子量为3000Da的透析袋透析12-36h,真空干燥2-3h得到五味子粗多糖;
(2)五味子多糖的羧甲基化:将五味子粗多糖溶于异丙醇溶液中,搅拌使其充分溶解,五味子粗多糖和异丙醇料液比为1:30-1:40(g/mL),溶解温度为20-25℃,搅拌时间为15-20min,搅拌速度为60-240r/min,向溶解后的五味子多糖溶液中加入质量分数为15-20%的NaOH溶液进行碱化,NaOH溶液的加入量为异丙醇体积的20-30%,碱化温度为20-25℃,碱化时间为1-2h,然后在搅拌状态下继续向碱化后的五味子粗多糖反应液中加入氯乙酸进行羧甲基化,氯乙酸加入量为0.005-0.08g/mL,水浴温度为40-80℃,羧甲基化反应时间为1-8h,待反应液冷却后调节反应液pH至中性,采用乙醇醇沉,离心后得到醇沉产物,将醇沉产物采用少量蒸馏水复溶后进行透析,透析结束后进行真空干燥得到羧甲基化五味子粗多糖;
(3)纯化:将步骤(2)得到的羧甲基化五味子粗多糖溶解于0.05-0.1mol/L的NaCl溶液中,然后缓慢滴加至DEAE-52层析柱中,并采用0.05-0.2mol/L的NaCl溶液进行梯度洗脱,绘制洗脱曲线,根据洗脱曲线分别收取合并洗脱液,得到羧甲基化五味子多糖不同组分,选取0.05mol/L NaCl的洗脱组分合并,经截留分子量为3000Da的透析袋透析、真空干燥后,得到羧甲基化五味子多糖。
进一步的,所述步骤(1)中五味子粗多糖的得率为15.9-19.8%,多糖含量为54.4-65.7%,溶解度为0.08-0.12mg/mL。
进一步的,所述步骤(2)中羧甲基化五味子粗多糖的得率为60.2-86.4%,羧甲基化取代度为0.41-0.71,溶解度为0.46-0.54mg/mL。
进一步的,所述步骤(1)中回流脱脂的温度为70-80℃,脱脂时间为1-2h,水提温度为90-100℃,提取时间为4-6h。
进一步的,所述步骤(2)中采用80%乙醇醇沉24-48h,醇沉液以4000-5000rpm转速离心5-10min。
进一步的,所述步骤(2)中采用经截留分子量为3000Da的透析袋透析首先采用流水透析,最后进行蒸馏水透析,流水透析时间为36-48h,蒸馏水透析时间为24-36h。
进一步的,所述步骤(2)中真空干燥时间为2-3h,温度为20-25℃,真空度为-0.085--0.1Mpa。
进一步的,所述步骤(3)中羧甲基化五味子粗多糖在NaCl溶液中经震荡加热溶解,震荡水浴的温度为50-60℃,震荡频率为120-160次/分,震荡溶解的时间10-12h,然后对溶解后的溶液进行离心分离,溶液离心的转速为:4000-5000r/min,离心时间为8-10min。
进一步的,所述步骤(3)中流水透析时间为36-48h,蒸馏水透析时间为24-36h,真空干燥时间为2-3h,真空干燥温度为20-25℃,真空干燥真空度为-0.085--0.1MPa。
进一步的,所述羧甲基化五味子多糖能够作为免疫增强剂用于功能食品和食品添加剂中。
本发明制备方法简单,步骤易于操作,采用分子修饰的方法制备出羧甲基化五味子粗多糖和羧甲基化五味子多糖;采用本发明中的制备方法得到的羧甲基化五味子多糖的得率和取代度均较高,溶解性好,溶解度分别是原五味子多糖的5倍和125倍,制备得到的羧甲基化五味子多糖能够有效改善持久性有机污染物PCB126的免疫抑制作用,能够作为免疫增强剂,应用于功能食品和食品添加剂。
附图说明
图1为反应温度、反应时间、氯乙酸终浓度之间相互作用对羧甲基化五味子多糖得率影响的响应面图(A、B、C)及等高线图(D、E、F)。
图2为反应温度、反应时间、氯乙酸终浓度之间相互作用对羧甲基化五味子多糖取代度影响的响应面图(A、B、C)及等高线图(D、E、F)。
图3为五味子多糖的红外光谱图。
图4为羧甲基化五味子多糖的红外光谱图。
图5为羧甲基化五味子多糖的原子力二维图(A)、三维图(B)和分子链高度分布图(C)。
图6为羧甲基化五味子多糖对PCB126染毒小鼠脾脏指数的影响图,ap<0.05,与空白对照组相比;bp<0.05,与模型组相比;cp<0.05,与CSP1高剂量组相比。
图7为羧甲基化五味子多糖对PCB126染毒小鼠胸腺指数的影响图,ap<0.05,与空白对照组相比;bp<0.05,与模型组相比;cp<0.05,与CSP1高剂量组相比。
图8为羧甲基化五味子多糖对PCB126染毒小鼠血清TNF-α水平的影响图,ap<0.05,与空白对照组相比;bp<0.05,与模型组相比。
图9为羧甲基化五味子多糖对PCB126染毒小鼠血清INF-γ水平的影响图,ap<0.05,与空白对照组相比;bp<0.05,与模型组相比。
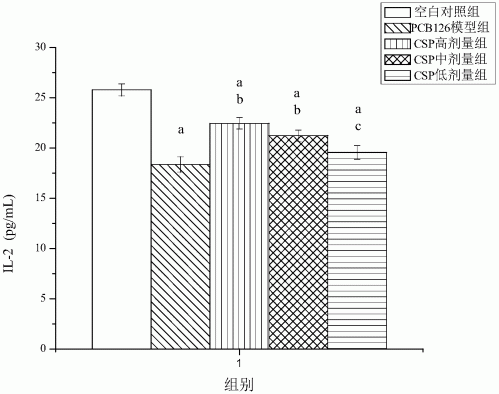
图10为羧甲基化五味子多糖对PCB126染毒小鼠血清IL-2水平的影响图,ap<0.05,与空白对照组相比;bp<0.05,与模型组相比;cp<0.05,与CSP1高剂量组相比。
具体实施方式
五味子粗多糖的制备
实施例1:
将新鲜五味子于55℃烘箱内干燥12h后进行粉碎,采用石油醚对干燥后的五味子于70℃回流脱脂1h,进行2次回流脱脂,然后将脱脂后的五味子药渣以料液比1:10(g/mL)加入蒸馏水进行水提,于90℃水提4h,提取2次,提取液合并经过减压浓缩后,80%乙醇反复醇沉3次,离心后,上清液经截留分子量为3000Da的透析袋透析12h、真空干燥2h,制得五味子粗多糖,多糖得率为15.9±0.3%,多糖含量为54.4±2.7%。
实施例2
将新鲜五味子于65℃烘箱内干燥24h后进行粉碎,采用石油醚对干燥后的五味子于80℃回流脱脂2h,进行3次回流脱脂,然后将脱脂后的五味子药渣以料液比1:15(g/mL)加入蒸馏水进行水提,于100℃水提6h,提取3次,提取液合并经过减压浓缩后,80%乙醇反复醇沉4次,离心后,上清液经截留分子量为3000Da的透析袋透析36h、真空干燥3h,制得五味子粗多糖,多糖得率为19.8±0.9%,多糖含量为65.7±2.7%,溶解度为0.10±0.02mg/mL。
以实施例2制备的五味子粗多糖为下一步的原料。
与现有文献中五味子多糖制备工艺相比(赵婷.五味子多糖的分离纯化、结构表征及其活性研究[D].江苏大学,2009.),该粗多糖的制备工艺采用80%乙醇反复醇沉3-4次,显著提高了五味子粗多糖的多糖含量,多糖含量提高了约21%左右;而采用真空干燥法可有效缩短干燥时间,干燥时间减少了约93%左右,该干燥方法可节约能源,有利于工业生产中的应用。
羧甲基化五味子粗多糖的制备
实施例3:
称取五味子粗多糖样品与异丙醇以料液比1:30(g/mL)混合,于20℃下,以转速为60r/min机械搅拌15min,进行充分溶解;向溶解后的五味子多糖溶液中加入质量分数为15%的NaOH溶液进行碱化,NaOH溶液的加入量为异丙醇体积的20%,温度20℃下继续机械搅拌1h;再加入氯乙酸于上述反应液内,使氯乙酸浓度达到0.005g/mL,置于40℃恒温水浴锅中,继续机械搅拌反应1h,冷却后用盐酸将反应产物调至中性,经80%乙醇醇沉24h,醇沉液以4000rpm转速离心5min后,沉淀经复溶,经截留分子量为3000Da的透析袋流水透析36h,蒸馏水透析24h后,于20℃、真空度-0.085MPa下真空干燥2h,即得羧甲基化五味子粗多糖(CSP),多糖得率为75.9±1.1%,羧甲基化取代度为0.41±0.02。
实施例4:
称取五味子粗多糖样品与异丙醇以料液比1:35(g/mL)混合,于25℃下,以转速为240r/min机械搅拌20min,进行充分溶解;向溶解后的五味子多糖溶液中加入质量分数为20%的NaOH溶液进行碱化,NaOH溶液的加入量为异丙醇体积的25%,温度25℃下继续机械搅拌2h;再加入氯乙酸于上述反应液内,使氯乙酸浓度达到0.02g/mL,置于60℃恒温水浴锅中,继续机械搅拌反应4h,冷却后用盐酸将反应产物调至中性,经80%乙醇醇沉36h,醇沉液以4000rpm转速离心10min后,沉淀经复溶,经截留分子量为3000Da的透析袋流水透析48h,蒸馏水透析36h后,于25℃、真空度-0.1MPa下真空干燥3h,即得羧甲基化五味子粗多糖(CSP),多糖得率为多糖得率为86.4±1.5%,羧甲基化取代度为0.71±0.03,溶解度为0.50±0.04mg/mL。
实施例5:
称取五味子粗多糖样品与异丙醇以料液比1:40(g/mL)混合,于25℃下,以转速为240r/min机械搅拌20min,进行充分溶解;向溶解后的五味子多糖溶液中加入质量分数为20%的NaOH溶液进行碱化,NaOH溶液的加入量为异丙醇体积的30%,温度25℃下继续机械搅拌2h;再加入氯乙酸于上述反应液内,使氯乙酸浓度达到0.08g/mL,置于80℃恒温水浴锅中,继续机械搅拌反应8h,冷却后用盐酸将反应产物调至中性,经80%乙醇醇沉48h,醇沉液以5000rpm转速离心10min后,沉淀经复溶,经截留分子量为3000Da的透析袋流水透析48h,蒸馏水透析36h后,于25℃、真空度-0.1MPa下真空干燥3h,即得羧甲基化五味子粗多糖(CSP),多糖得率为60.2±2.2%,羧甲基化取代度为0.68±0.02。
响应面法优化羧甲基化五味子粗多糖合成工艺
以单因素实验为基础,反应温度选取50℃、60℃和70℃三个水平,反应时间选取2h、4h和6h三个水平,氯乙酸终浓度选取0.01g/mL、0.02g/mL和0.04g/mL三个水平,利用Design Expert 8.0软件根据Box-Benhnken中心组合设计原理进行实验设计,以反应温度(A)、反应时间(B)和氯乙酸终浓度(C)为自变量,以CSP的得率(Y1)和取代度(Y2)为响应值,采用响应曲面法来优化五味子粗多糖羧甲基化工艺条件。响应面实验因素水平见表1,响应面分析结果见表2、表3及表4。
表1:实验因素水平表
表2:响应面实验设计方案及响应值结果
表3得率的方差分析表
注:P<0.0001为极显著,P<0.05为显著。
采用Design-Expert 8软件对实验数据进行回归分析,按照各因素对得率试验结果的影响进行二次方程拟合,拟合得到下式:
Y1=–84.48711+2.53102A+28.50936B+67.94377C-0.036938AB+0.21919AC–1.66175BC–0.020539A2–2.94075B2–36.32919C2
公式中Y1为得率。
各因子对CSP的得率均具有较显著的影响(P<0.05)。三个因素对于得率的影响顺序为:氯乙酸终浓度>反应温度>反应时间。试验模型P值<0.0001,证明模型显著。失拟误差值不显著(F值=2.14;P值=0.2374),说明检验结果与模型计算结果没有显著差异,可用于五味子多糖羧甲基化合成实验的理论预测。
表4:羧甲基化五味子多糖取代度的方差分析
注:P<0.0001为极显著,P<0.05为显著
采用Design-Expert 8软件对实验数据进行回归分析,按照各因素对取代度试验结果的影响进行二次方程拟合,拟合得到下式:
Y2=-0.68299+0.026417A+0.14229B+0.45287C+4.6875×10-3AB+4.00000×10-3AC–4.84211×10-3BC–2.26187×10-3A2–0.018494B2–0.18924C2
公式中Y2为取代度。
各因子对CSP的取代度具有较显著的影响(P<0.05)。三个因素对于取代度的影响顺序为:氯乙酸终浓度>反应时间>反应温度。试验模型的P值<0.0001,证明模型显著。失拟误差值不显著(F值=6.37;P值=0.0528),说明检验结果与模型计算结果没有显著差异,表明回归模型与实际情况拟合很好,可用于五味子多糖羧甲基化合成实验的理论预测。
利用Design Expert 8.0软件根据多元回归方程进行绘图分析,得到回归方程的响应面图(见图1和图2)三个因素对于CSP的得率和取代度均具有显著的影响,其中氯乙酸终浓度的影响最显著。
(5)实验结果分析与优化:
采用Design-Expert 8软件对实验数据进行回归分析计算,得到合成CSP的最佳工艺条件为:反应温度为63℃,反应时间为4.5h,氯乙酸终浓度为0.022g/mL。在该条件下,平行实验5次,得到CSP的得率为88.3±1.65%,取代度为0.72±0.022。实际测定值与响应面模型预测结果较为接近,说明该响应面法优化得到的模型准确可靠,适用于五味子粗多糖羧甲基化的修饰。与2011年,仰榴青等申请的专利“一种羧甲基化黑木耳多糖、粗多糖及其制备方法和应用”(申请号:CN201110219047.3)相比,该工艺条件中氯乙酸用量降低了46%,氯乙酸用量的降低可减少反应过程中多糖降解副反应的发生,使得羧甲基化多糖得率显著提高,提高了约30%左右;其次,该工艺条件中选用机械搅拌代替磁力搅拌,搅拌强度大,混合效果好,易于调节和操作,更适用于羧甲基化五味子多糖的大量制备;而采用真空干燥法可有效缩短干燥时间,节约能源,有利于工业生产中的应用。
实施例6:
采用响应面得到的最佳工艺参数反应温度为63℃,反应时间为4.5h,氯乙酸终浓度为0.022g/mL,制备得到羧甲基化五味子粗多糖。
羧甲基化五味子粗多糖的纯化及结构特征
称取上述实施例6中制备羧甲基化五味子粗多糖(CSP)0.5g,进行羧甲基化五味子粗多糖的纯化。
实施例7:
溶于0.05mol/LNaCl溶液,于震荡频率为160次/分、温度50℃的震荡恒温水浴中充分溶 解10h,溶解液经4000r/min离心10min,除去不溶物后,上清液通过DEAE-52离子交换柱(2.0×50cm)进行分离;以0.05、0.1、0.15和2mol/L的NaCl溶液洗脱,用自动收集器逐管收集洗脱液,将恒流泵的流速控制在1mL/min,每管收集5mL。收集液用硫酸-苯酚法逐管检测,根据洗脱曲线分别收取合并洗脱液,其中0.05mol/L NaCl的洗脱液经减压浓缩,截留分子量为3000Da的透析袋流水透析48h、蒸馏水透析24h后,于温度20℃、真空度为-0.085MPa的真空干燥箱内干燥2h,得到羧甲基化五味子多糖组分(CSP1)。
实施例8:
溶于0.08mol/LNaCl溶液,于震荡频率为150次/分、温度55℃的震荡恒温水浴中充分溶解11h,溶解液经4500r/min离心9min,除去不溶物后,上清液通过DEAE-52离子交换柱(2.0×50cm)进行分离;以0.05、0.1、0.15和2mol/L的NaCl溶液洗脱,用自动收集器逐管收集洗脱液,将恒流泵的流速控制在1mL/min,每管收集5mL。收集液用硫酸-苯酚法逐管检测,根据洗脱曲线分别收取合并洗脱液,其中0.05mol/L NaCl的洗脱液经减压浓缩,截留分子量为3000Da的透析袋流水透析40h、蒸馏水透析30h后,于温度21℃、真空度为-0.090MPa的真空干燥箱内干燥2.5h,得到羧甲基化五味子多糖组分(CSP1)。
实施例9:
溶于0.1mol/LNaCl溶液,于震荡频率为120次/分、温度60℃的震荡恒温水浴中充分溶解12h,溶解液经5000r/min离心8min,除去不溶物后,上清液通过DEAE-52离子交换柱(2.0×50cm)进行分离;以0.05、0.1、0.15和2mol/L的NaCl溶液洗脱,用自动收集器逐管收集洗脱液,将恒流泵的流速控制在1mL/min,每管收集5mL。收集液用硫酸-苯酚法逐管检测,根据洗脱曲线分别收取合并洗脱液,其中0.05mol/L NaCl的洗脱液经减压浓缩,截留分子量为3000Da的透析袋流水透析36h、蒸馏水透析36h后,于温度25℃、真空度为-0.1MPa的真空干燥箱内干燥3h,得到羧甲基化五味子多糖组分(CSP1)。
与现有文献(赵婷.五味子多糖的分离纯化、结构表征及其活性研究[D].江苏大学,2009.)和专利(申请号:CN201110219047.3及CN201210132340.0)相比,该纯化过程中多糖经恒温震荡进行充分溶解,减少了羧甲基化五味子多糖原料的浪费;而柱纯化过程采用直径较大的离子交换柱,使得上样量增加了一倍,在不改变纯化效果的基础上显著加快了纯化速度;而采用真空干燥法可有效缩短干燥时间,节约能源,有利于工业生产中的应用。
取实施例8制备得到羧甲基化五味子多糖(CSP1),溶解度为12.50mg/mL。
据2005版药典进行溶解度的测定,五味子粗多糖的溶解度为0.10±0.03mg/mL,羧甲基化五味子粗多糖的溶解度为0.50±0.04mg/mL,羧甲基化五味子多糖(CSP1)的溶解度为12.50 ±0.26mg/mL。
分子量的测定:采用高效凝胶尺寸排阻色谱-多角度激光光散射仪-示差折光检测仪联用分析法(HPSEC-MALLS-RI System)对多糖相对分子质量进行测定。色谱条件以TSK-GEL系列G6000PWXL和G4000PWXL色谱柱(300mm,7.8mm,TOSOH,日本)为分析柱,以0.15mol/L NaNO3和0.05mol/L NaH2PO4(pH=7)为流动相,在柱温为35℃的条件下,以0.5mL/min的流速进行洗脱分析。将CSP1样品配制成质量浓度为5mg/mL的溶液,经12000r/min的高速离心机离心10min后取上清液过膜后进样100μL。CSP1分子量为1.698×104Da。与现有文献(赵婷.五味子多糖的分离纯化、结构表征及其活性研究[D].江苏大学,2009.)和专利(申请号:CN201110219047.3及CN201210132340.0)相比,CSP1分子量较小,而分子量较小的多糖溶解度高且更易于其活性作用的发挥。
单糖组成分析:精密称取多糖样品5mg于安瓿瓶中,用2mol/L的硫酸溶液溶解,封口,100℃烘箱中加热水解8h后,水解液加碳酸钡中和至中性,以4000r/min离心除去BaSO4沉淀,上清液冷冻干燥。水解产物经乙酰化后用岛津GC 2010气相色谱系统分析。CSP1的单糖组成为:甘露糖、葡萄糖和半乳糖,其摩尔比为1:44.84:3.71。可见CSP1由三种单糖组成,分别为甘露糖、葡萄糖和半乳糖,而现有文献(赵婷.五味子多糖的分离纯化、结构表征及其活性研究[D].江苏大学,2009.)和专利(CN201210132340.0)中,五味子多糖由六种单糖构成(鼠李糖、阿拉伯糖、木糖、甘露糖、葡萄糖和半乳糖)。
红外测定:以溴化钾(KBr)压片法,取一定量的干燥的多糖样品,采用傅立叶变换红外光谱仪(ATAVAR360)扫描4000~400cm-1波长段进行结构表征。五味子多糖经羧甲基化后的多糖于1600cm-1、1420cm-1处均出现强吸收峰,(为-COO-的特征吸收峰,其中1600cm-1左右处为-C-O-的非对称伸缩振动吸收峰,1420cm-1左右处为-C-O-的对称伸缩振动吸收峰),表明羧甲基化成功。
原子力电镜:将多糖样品配制成1mg/mL的溶液,过膜并收集滤液,取20μL滤液使其均匀附着在干净的云母片上,室温下防灰干燥。用扫描探针显微镜(MFP-3D)对样品进行观测。在水溶液中呈聚集状,分子链的厚度在0.1-1nm。与现有文献(赵婷.五味子多糖的结构、生物活性及其免疫机制研究[D].江苏大学,2013.)相比,羧甲基化五味子多糖在水溶液中的聚集减少,且多糖链厚度较五味子多糖组分(1-5nm)显著降低。
羧甲基化五味子多糖对PCB126致机体免疫毒性的干预作用
实验动物
ICR小鼠(清洁级),雌雄各半,体重为20±2g,购于江苏大学动物实验中心,实验之前检疫3天,饲养温度范围为21±1℃,饲养湿度范围为60±5%。
材料与试剂
取实施例8纯化得到的羧甲基化五味子多糖;
PCB126、生理盐水、苦味酸;
TNF-α酶联免疫试剂盒、IL-2酶联免疫试剂盒、IFN-γ酶联免疫试剂盒。
实验分组与给药
于实验前适应喂养70只ICR小鼠3天后,随机分成5组,每组14只,雌雄各半并分开喂养,设置空白对照组、PCB126模型组、羧甲基化五味子多糖组分(CSP1)高、中、低三种浓度剂量组。每天给药1次,连续14天。而于给药第7天,PCB126模型组、CSP1高、CSP1中、CSP1低三种浓度剂量组同时灌胃给予50μg/kg PCB126(灌胃量均为每只0.1mL),持续给毒5天。
分组、剂量和给药途径如下:
空白对照组:每天灌胃相同剂量的生理盐水(0.1mL/20g/d),进食和饮水自由;
PCB126模型组:每天灌胃相同剂量的生理盐水(0.1mL/20g/d),于第7天开始灌胃给予PCB126,给予5天,进食和饮水自由;
CSP1给药组:分高、中、低三种浓度剂量组,
CSP1高剂量组:每天分别灌胃相同剂量的CSP1(400mg/kg/d),于给药第7天开始灌胃给予PCB126,给予5天,进食和饮水自由;
CSP1中剂量组:每天分别灌胃相同剂量的CSP1(200mg/kg/d),于给药第7天开始灌胃给予PCB126,给予5天,进食和饮水自由;
CSP1低剂量组:每天分别灌胃相同剂量的CSP1(100mg/kg/d),于给药第7天开始灌胃给予PCB126,给予5天,进食和饮水自由。
(1)免疫器官指数
末次给药后,于次日禁食8h,称量动物体重并记录。摘除眼球取血后处死,取出胸腺、脾脏经生理盐水清洗后用滤纸吸干,称重并记录。按下式计算各脏器指数:
(2)血液指标
用ELISA酶联免疫试剂盒测定小鼠血清中IL-2、INF-γ、TNF-α的含量。
统计学处理
用SPSS16.0统计软件对数据进行分析。结果表示为 组间差异采用单因素方差分析(One-way ANOVA),采用Tukey检验法比较各组间差异显著性,P﹤0.05表示有显著性差异。实验结果
CSP1对染毒小鼠的脾脏指数、胸腺指数分别见图6和图7。与空白对照组相比,模型组的小鼠脾脏和胸腺指数显著下降(P<0.05),说明PCB126致小鼠免疫抑制模型建立成功;而CSP1高、中、低剂量均不同程度上恢复了小鼠的脾脏和胸腺指数,其中CSP1高剂量组可同时显著提高小鼠脾脏指数与胸腺指数。CSP1对染毒小鼠血清中TNF-α、IFN-γ、IL-2水平的影响分别见图8、图9和图10。与空白对照组相比,模型组的小鼠血清中TNF-α、IFN-γ和IL-2水平均显著下降(P<0.05),而CSP1高、中、低剂量小鼠血清中TNF-α、IFN-γ和IL-2含量均有不同程度的上升,其中CSP1高剂量组小鼠血清中的TNF-α的含量较模型组显著上升(P<0.05),且CSP1高剂量组和中剂量小鼠血清中IL-2的含量较模型组显著上升(P<0.05)。目前,现有文献报道,五味子多糖(赵婷.五味子多糖的结构、生物活性及其免疫机制研究[D].江苏大学,2013.)与黑木耳多糖(宋广磊.黑木耳多糖的分离制备及生物活性研究[D].浙江工商大学,2011.)具有免疫调节活性,可显著改善环磷酰胺所致的免疫抑制作用,但对于持久性有机污染物PCB126所致机体免疫毒性的干预作用未见相关报道。
一种羧甲基化五味子多糖及其制备方法和应用专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0