IPC分类号 : C07F19/00,C09K11/06,H01L51/50,H01L51/54,H01L51/56
专利摘要
本发明涉及一种离子型磷光金属配合物及其制备方法和用途,所述配合物的结构为:[PtM3{(PPh2CH2)3P}(C≡CR)}(C≡CR’)(μ‑Cl)]2+An‑2/n;其中,M选自Au(I)或Ag(I);R、R'相同或不同,彼此独立地选自:烷基、烯基、炔基、芳基、杂芳基;所述的烷基、烯基、炔基、芳基、杂芳基均可被一个或多个取代基取代,所述取代基选自烷基、烯基、炔基、烷氧基、氨基、卤素、卤烷基、芳基、杂芳基;所述取代基任选进一步被如下一个或多个基团取代:烷基、烷氧基、氨基、卤素、卤代烷基、芳基、杂芳基;An‑为一价或二价阴离子,n为1或2;μ‑代表桥联。以所述配合物为发光层掺杂体,制备得到的有机发光二极管,外量子效率大于10%,可应用于平板显示和日常照明领域中。
权利要求
1.下式(I)所示的磷光PtM3异四核金属有机炔配合物,
[PtM3{(PPh2CH2)3P}(C≡CR)}(C≡CR')(μ-Cl)]2+An-2/n; (I)
其中,M选自Au(I)或Ag(I);
R、R'相同或不同,彼此独立地选自:烷基、烯基、炔基、芳基、杂芳基;所述的烷基、烯基、炔基、芳基、杂芳基均可被一个或多个取代基取代,所述取代基选自烷基、烯基、炔基、烷氧基、氨基、卤素、卤代烷基、芳基、杂芳基;
所述取代基任选进一步被如下一个或多个基团取代:烷基、烷氧基、氨基、卤素、卤代烷基、芳基、杂芳基;
An-为一价或二价阴离子,n为1或2;μ-代表桥联。
2.根据权利要求1所述的配合物,其特征在于,所述阴离子选自如下:ClO4-、PF6-、SbF6-、BF4-、B(C6H5)4-、CF3SO3-、或SiF62-;
优选地,所述R、R'相同或不同,彼此独立地选自:烷基、芳基、杂芳基、-芳基-杂芳基、-杂芳基-芳基、-芳基-芳基、-杂芳基-杂芳基;所述的烷基、芳基、杂芳基可被如下一个或多个取代基取代:烷基、烯基、炔基、烷氧基、氨基、芳基、杂芳基;所述芳基为苯基、萘基、菲基等;所述杂芳基可为含N杂芳基,例如咪唑基、苯并咪唑基、萘并咪唑基、菲并咪唑基、咔唑基、吩噻嗪基、喹啉基、咔唑基等;
还优选地,所述R、R'相同或不同,彼此独立地选自:芳基、咔唑基、吩噻嗪基、喹唑啉基、芳基咔唑基、咔唑基芳基、芳基并咪唑基、芳基并咪唑基芳基;上述基团定义中的芳基、咔唑基、吩噻嗪基、喹唑啉基、芳基并咪唑基可任选被一个或多个取代基取代;所述取代基选自烷基、烷氧基、卤素、卤代烷基、芳基、咔唑基、吩噻嗪基、喹唑啉基、-NH-芳基、-N(芳基)2、芳基并咪唑基、咪唑基;
优选的,所述R、R'相同或不同,彼此独立地选自:咔唑基芳基、烷基芳基、烷基咔唑基、芳基咔唑基、咔唑基芳基咔唑基、N-烷基吩噻嗪基、二芳基氨基芳基、N-芳基-菲并咪唑基芳基、或N-芳基-苯并咪唑基芳基。
3.根据权利要求1或2所述的配合物,其特征在于,所述配合物的立体结构如下:
4.根据权利要求1-3任一项所述的配合物,其特征在于,所述配合物选自如下:
其中,虚线表示的化学键为连接键。
5.根据权利要求1-4任一项所述配合物的制备方法,其特征在于,包括如下步骤:将(Ph2PCH2)3P、[M(tht)](An-)、(NH4)(An-)和Pt(PPh3)2(C≡CR)(C≡CR')在溶剂中反应,得到所述配合物;
其中,所述tht(tetrahydrothiophene)为四氢噻吩,An-、M、R、R'具有权利要求1-4中任一项所述定义。
6.根据权利要求5所述的制备方法,其特征在于,所述溶剂为卤代烃;
优选地,(Ph2PCH2)3P:[M(tht)](An-):(NH4)(An-):Pt(PPh3)2(C≡CR)(C≡CR')的摩尔比为1.0~2.5:1.5~4.0:1.5~4.0:0.5~1.5,还优选摩尔比为2:3:3:1。
7.根据权利要求1-4任一项所述配合物的用途,其特征在于,用于制备有机发光二极管。
8.一种有机发光二极管,其特征在于,包括发光层,其中所述发光层中含有权利要求1-4任一项所述的配合物;
优选地,在所述发光层中,所述配合物占有机发光二极管发光层所有材料重量百分比为1-20%,更优选2-8%,进一步优选3%;
优选地,所述有机发光二极管的器件结构为:ITO/PEDOT:PSS(50nm)/48.5%mCP:48.5%OXD-7:3%wt权利要求1-4任一项所述的配合物(50nm)/BmPyPB(50nm)/LiF(1nm)/Al(100nm);其中ITO为氧化铟锡导电薄膜。
9.权利要求8所述有机发光二极管的制备方法,其特征在于,包括:
1)采用溶液法在阳极上制备有机发光二极管中的空穴注入层;
2)采用溶液法制备掺杂有权利要求1-4中任一项所述配合物的发光层;
3)再依次利用真空热蒸镀方法制备电子传输层、电子注入层、以及阴极层;优选地,所述方法采用如下步骤:首先利用水溶性PEDOT:PSS制备空穴注入层;其次利用具有空穴传输特性的mCP和具有电子传输特性的OXD-7为混合主体材料,与权利要求1-4任一项所述的配合物掺杂制备发光层;再依次利用真空热蒸镀方法制备Bmpypb电子传输层、LiF电子注入层、以及Al阴极层。
10.权利要求8所述有机发光二极管的用途,其特征在于,用于平板显示和日常照明领域中。
说明书
技术领域
本发明属于磷光材料与有机发光二极管领域,具体涉及一种磷光PtM3异四核金属有机炔配合物及其制备方法和用途。
背景技术
有机发光二极管(OLED)是一种具有夹心结构的薄膜发光器件,能够在3-12V低电压作用下将电能转化为光能,即电致发光,其在平板显示和照明领域具有非常广阔的应用。有机发光二极管的核心是发光材料,目前商用磷光材料绝大多数是电中性环金属铱(III)配合物,将其掺杂于有机主体材料中组成发光层,其最大优势是便于真空热蒸镀制作理想的薄膜发光层。但存在价格昂贵、色度不全(蓝色磷光材料缺乏)、铱资源紧缺、难于制备大尺寸器件等挑战性问题。与电中性化合物相比,离子型磷光金属配合物制备更简单、廉价,稳定性更好,而且易溶于有机溶剂,适合于大面积溶液旋涂或喷墨印刷成膜,能够大幅度降低器件制备成本。
发明内容
为解决上述问题,本发明提供一种磷光PtM3异四核金属有机炔配合物及其制备方法和用途。
本发明通过如下方式实现:
下式(I)所示的磷光PtM3异四核金属有机炔配合物,
[PtM3{(PPh2CH2)3P}(C≡CR)}(C≡CR')(μ-Cl)]2+An-2/n; (I)
其中,M选自Au(I)或Ag(I);
R、R'相同或不同,彼此独立地选自:烷基、烯基、炔基、芳基、杂芳基;所述的烷基、烯基、炔基、芳基、杂芳基均可被一个或多个取代基取代,所述取代基选自烷基、烯基、炔基、烷氧基、氨基、卤素、卤代烷基、芳基、杂芳基;
所述取代基任选进一步被如下一个或多个基团取代:烷基、烷氧基、氨基、卤素、卤代烷基、芳基、杂芳基;
An-为一价或二价阴离子,n为1或2;μ-代表桥联。
根据本发明,所述阴离子选自如下:ClO4-、PF6-、SbF6-、BF4-、B(C6H5)4-、CF3SO3-、SiF62-等;
在本发明的一个技术方案中,R、R'相同或不同,彼此独立地选自:烷基、芳基、杂芳基、-芳基-杂芳基、-杂芳基-芳基、-芳基-芳基、-杂芳基-杂芳基;上述所述的烷基、芳基、杂芳基可被如下一个或多个取代基取代:烷基、烯基、炔基、烷氧基、氨基、芳基、杂芳基;
在本发明的一个技术方案中,所述芳基为苯基、萘基、菲基等;所述杂芳基可为含N杂芳基,例如咪唑基、苯并咪唑基、萘并咪唑基、菲并咪唑基、咔唑基、吩噻嗪基、喹啉基、咔唑基等;
在本发明的一个技术方案中,所述R、R'相同或不同,彼此独立地选自:芳基、咔唑基、吩噻嗪基、喹唑啉基、芳基咔唑基、咔唑基芳基、芳基并咪唑基、芳基并咪唑基芳基;上述基团定义中的芳基、咔唑基、吩噻嗪基、喹唑啉基、芳基并咪唑基可任选被一个或多个取代基取代;所述取代基选自烷基、烷氧基、卤素、卤代烷基、芳基、咔唑基、吩噻嗪基、喹唑啉基、-NH-芳基、-N(芳基)2、芳基并咪唑基、咪唑基;
在本发明的一个技术方案中,所述R、R'相同或不同,彼此独立地选自:咔唑基芳基、烷基芳基、烷基咔唑基、芳基咔唑基、咔唑基芳基咔唑基、N-烷基吩噻嗪基、二芳基氨基芳基、N-芳基-菲并咪唑基芳基、或N-芳基-苯并咪唑基芳基。
根据本发明,所述式(I)所示的磷光PtM3异四核金属有机炔配合物的立体结构如下:
根据本发明,所述式(I)所示的磷光PtM3异四核金属有机炔配合物具体的结构优选如下:
其中,虚线表示的化学键为连接键。
本发明还提供如上所述式(I)所示的磷光PtM3异四核金属有机炔配合物的制备方法,包括如下步骤:将(Ph2PCH2)3P、[M(tht)](An-)、(NH4)(An-)和Pt(PPh3)2(C≡CR)(C≡CR')在溶剂中反应,得到所述式(I)所示的配合物;
其中,所述tht(tetrahydrothiophene)为四氢噻吩,An-、M、R、R'如上所定义。
根据本发明,所述溶剂优选为卤代烃,例如二氯甲烷。
根据本发明,在所述方法中,(Ph2PCH2)3P:[M(tht)](An-):(NH4)(An-):Pt(PPh3)2(C≡CR)(C≡CR')的摩尔比为1.0~2.5:1.5~4.0:1.5~4.0:0.5~1.5,优选摩尔比为2:3:3:1。
根据本发明,所述反应在室温下进行。
优选地,反应结束后,用硅胶柱色谱分离提纯式(I)所示的配合物。
本发明所述式(I)所示的磷光PtM3异四核金属有机炔配合物在固体粉末和薄膜中均具有强磷光发射,其磷光量子产率在薄膜中高于60%;并且其发射光颜色分布较宽,从蓝绿到橙红。故其可以作为发光层掺杂体,用于有机发光二极管的制备。
本发明还提供了式(I)所示的磷光PtM3异四核金属有机炔配合物的用途,其用于制备有机发光二极管。
本发明还提供了一种有机发光二极管,包括发光层,其中所述发光层中含有所述式(I)所示的配合物。
根据本发明,在所述发光层中,所述式(I)所示的配合物优选占有机发光二极管发光层所有材料的1-20%(重量百分比),更优选2-8%,进一步优选3%。
根据本发明,所述有机发光二极管的结构可以为现有技术中已知的各种结构。优选包括:阳极层、空穴注入层、发光层、电子传输层、电子注入层、阴极层。
所述有机发光二极管还进一步包括基板(例如玻璃基板)。
所述阳极可为铟锡氧化物(ITO);
所述空穴注入层可为PEDOT:PSS(PEDOT:PSS=聚(3,4-亚乙二氧基噻吩)-聚(苯乙烯磺酸))。
所述发光层含有式(I)所示的配合物,以及具有空穴传输特性的物质和/或具有电子传输特性的物质。
其中,具有空穴传输特性的物质可以为2,6-DCZPPY(2,6-二(3-(9-咔唑)苯基)吡啶)、mCP(1,3-双(9-咔唑基)苯)、CBP(4,4'-二(9-咔唑)-1,1'-联苯)、或TCTA(三(4-(9-咔唑)苯基)胺)中的一种或多种;具有电子传输特性的物质可以为OXD-7(1,3-双(5-(4-(叔丁基)苯基)-1,3,4-噁二唑-2-基)苯);
所述电子传输层可为BmPyPB(3,3”,5,5”-四(3-吡啶基)-1,1':3',1”-三联苯)、TPBi(1,3,5-三(1-苯基-1H-苯并[d]咪唑-2-基)苯)、BCP(2,9-二甲基-4,7-二苯基-1,10-菲珞啉)或OXD-7中的一种或多种;
所述电子注入层为LiF,所述阴极为Al。
根据本发明,含有所述式(I)磷光配合物的器件结构优选为:ITO/PEDOT:PSS(50nm)/48.5%mCP:48.5%OXD-7:3%wt式(I)所示的配合物(50nm)/BmPyPB(50nm)/LiF(1nm)/Al(100nm);其中ITO为氧化铟锡导电薄膜,PEDOT:PSS为聚(3,4-亚乙二氧基噻吩)-聚(苯乙烯磺酸),mCP为(1,3-双(9-咔唑基)苯),OXD-7为1,3-双(5-(4-(叔丁基)苯基)-1,3,4-噁二唑-2-基)苯,BmPyPb为(3,3”,5,5”-四(3-吡啶基)-1,1':3',1”-三联苯)。
本发明还提供如上所述有机发光二极管的制备方法,包括:
1)采用溶液法在阳极上制备有机发光二极管中的空穴注入层;
2)采用溶液法制备掺杂有式(I)所示的配合物的发光层;
3)再依次利用真空热蒸镀方法制备电子传输层、电子注入层、以及阴极层。
在一个优选的实施方案中,对于所述式(I)磷光配合物,所述方法包括:首先利用水溶性PEDOT:PSS制备空穴注入层;其次利用具有空穴传输特性的mCP和具有电子传输特性的OXD-7为混合主体材料,与式(I)所示的配合物掺杂制备发光层;再依次利用真空热蒸镀方法制备Bmpypb电子传输层、LiF电子注入层、以及Al阴极层。
根据本发明,在所述方法中,PEDOT:PSS空穴注入层、mCP:OXD-7掺杂发光层分别利用溶液旋涂法制备薄膜,BmPyPb电子传输层和LiF电子注入层采用真空热蒸镀法制备薄膜。
由本发明的磷光配合物制备的有机发光二极管具有优异的性能,其具有较高的电-光转换效率。
本发明进一步提供了所述有机发光二极管的用途,其可以用于平板显示和日常照明领域中。
与现有技术相比,本发明具有如下优点:
1)本发明式(I)所示的配合物在固体和薄膜中均具有很强的磷光发射,薄膜中磷光量子效率高于60%甚至高达90%;
2)本发明首次利用式(I)所示的配合物为发光材料组装有机发光二极管,制备的有机发光二极管的外量子转换效率高于10%;
3)本发明利用正交溶液法制备有机发光二极管的空穴注入层和发光层,能够大幅度降低器件制备成本。
除非另有定义,否则本文所有科技术语具有的涵义与权利要求主题所属领域技术人员通常理解的涵义相同。应理解,上述简述和下文的详述为示例性且仅用于解释,而不对本申请主题作任何限制。在本申请中,除非另有说明,否则所用“或”、“或者”表示“和/或”。此外,所用术语“包括”以及其它形式,例如“包含”、“含”和“含有”并非限制性。
术语“烷基”指具有1-12个,优选1-10个碳原子的直链或支链烷基,所述烷基例如为甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、仲丁基、戊基、新戊基。
术语“烯基”应理解为优选表示直链或支链的烃基,其包含一个或多个双键并且具有2~12个碳原子,优选“C2-10烯基”。“C2-10烯基”应理解为优选表示直链或支链的一价烃基,其包含一个或多个双键并且具有2、3、4、5、6、7、8、9或10个碳原子,特别是2或3个碳原子(“C2-3烯基”),应理解,在所述烯基包含多于一个双键的情况下,所述双键可相互分离或者共轭。所述烯基是例如乙烯基、烯丙基、(E)-2-甲基乙烯基、(Z)-2-甲基乙烯基、(E)-丁-2-烯基、(Z)-丁-2-烯基、(E)-丁-1-烯基、(Z)-丁-1-烯基、戊-4-烯基、(E)-戊-3-烯基、(Z)-戊-3-烯基、(E)-戊-2-烯基、(Z)-戊-2-烯基、(E)-戊-1-烯基、(Z)-戊-1-烯基、己-5-烯基、(E)-己-4-烯基、(Z)-己-4-烯基、(E)-己-3-烯基、(Z)-己-3-烯基、(E)-己-2-烯基、(Z)-己-2-烯基、(E)-己-1-烯基、(Z)-己-1-烯基、异丙烯基、2-甲基丙-2-烯基、1-甲基丙-2-烯基、2-甲基丙-1-烯基、(E)-1-甲基丙-1-烯基、(Z)-1-甲基丙-1-烯基。
术语“炔基”应理解为表示直链或支链的一价烃基,其包含一个或多个三键并且具有2~12个碳原子,优选“C2-C10炔基”。术语“C2-C10炔基”应理解为优选表示直链或支链的烃基,其包含一个或多个三键并且具有2、3、4、5、6、7、8、9或10个碳原子,特别是2或3个碳原子(“C2-C3-炔基”)。所述炔基是例如乙炔基、丙-1-炔基、丙-2-炔基、丁-1-炔基、丁-2-炔基、丁-3-炔基、戊-1-炔基、戊-2-炔基、戊-3-炔基、戊-4-炔基、己-1-炔基、己-2-炔基、己-3-炔基、己-4-炔基、己-5-炔基、1-甲基丙-2-炔基、2-甲基丁-3-炔基、1-甲基丁-3-炔基、1-甲基丁-2-炔基、3-甲基丁-1-炔基。
术语“芳基”应理解为优选表示具有5~20个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环,优选“C6-14芳基”。术语“C6-14芳基”应理解为优选表示具有6、7、8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“C6-14芳基”),特别是具有6个碳原子的环(“C6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“C9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“C10芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“C13芳基”),例如芴基,或者是具有14个碳原子的环(“C14芳基”),例如蒽基。
术语“杂芳基”应理解为含有5-20个环原子、5-14个环原子,或5-12个环原子,或5-10个环原子,或5-6个环原子的单环、双环和三环体系,其中至少一个环体系是芳香族的,且至少一个环体系包含一个或多个杂原子(例如N、O、S、Se、B、Si、P等),其中每一个环体系包含5-7个原子组成的环,且有一个或多个连接点与分子其余部分相连。所述杂芳基基团任选地被一个或多个本发明所描述的取代基所取代。在一些实施方案中,5-10个原子组成的杂芳基包含1,2,3或4个独立选自O、S、Se和N的杂原子。在另一些实施方案中,5-6个原子组成的杂芳基包含1,2,3或4个独立选自O、S、Se和N的杂原子。
杂芳基基团的单环实例包括,但并不限于,噻吩基、呋喃基、吡咯基、噁唑基、噻唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、噁二唑基、三唑基、噻二唑基、噻-4H-吡唑基等以及它们的苯并衍生物,例如苯并呋喃基、苯并噻吩基、苯并噁唑基、苯并异噁唑基、苯并咪唑基、苯并三唑基、吲唑基、吲哚基、异吲哚基等;或吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基等,以及它们的苯并衍生物,例如喹啉基、喹唑啉基、异喹啉基等;或吖辛因基、吲嗪基、嘌呤基等以及它们的苯并衍生物;或噌啉基、酞嗪基、喹唑啉基、喹喔啉基、萘啶基、蝶啶基、咔唑基、吖啶基、吩嗪基、吩噻嗪基、吩噁嗪基等。
术语“氨基”应理解为基团-NR12,其中R1为H、C1-6烷基、芳基、杂芳基。
附图说明:
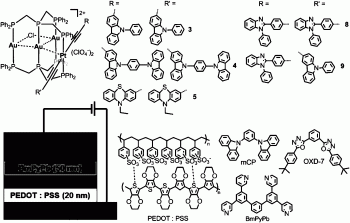
图1为实施例16制备得到的有机发光二极管器件结构示意图及制备有机发光二极管的部分有机材料化学结构。
具体实施方式:
为了使本发明的发明目的、技术方案和技术效果更加清晰,以下结合附图和实施例对本发明进行进一步详细说明。应当理解的是,本说明书中描述的实施例只是为了解释本发明,而非限定本发明。
如下实施例中Carb为咔唑基,4-C6H4Carb-9代表4-(9-9H-咔唑基)苯基,Ph代表苯基,C6H4But-4代表4-叔丁基-苯基,2-Carb-9-Ph代表9-苯基-9H-咔唑-2-基,3-CarbC6H4Carb-9代表4-(9H-咔唑-9-基)苯基-咔唑-3-基,3-PTZ-10-Et代表10-乙基-10H-吩噻嗪-3-基,4-C6H4NPh2代表4-二苯氨基-苯基,4-C6H4-phenim代表4-(1-苯基-1H-菲并[9,10-D]咪唑-2-基)-苯基,4-C6H4-2-benzimd-1-Ph代表4-(1-苯基-1H-苯并[d]咪唑-2-基)苯基,3-Carb-9-Ph代表9-苯基-9H-咔唑-3-基,2-Carb-9-Et代表9-乙基-9H-咔唑-2-基,tht代表四氢噻吩。
实施例1:配合物1的制备
向20mL溶解了Pt(PPh3)2(C≡C-4-C6H4Carb-9)2(62.6mg,0.05mmol)的二氯甲烷溶液中加入(Ph2PCH2)3P(62.8mg,0.1mmol)、Au(tht)Cl(48mg,0.15mmol)、NH4ClO4(18mg,0.15mmol)。反应液在室温下搅拌8小时后变为浅黄色。利用硅胶柱色谱纯化产物,使用CH2Cl2/MeOH(V/V=10:0.5)为洗脱液收集主产物。产率:68%。1H NMR(CDCl3,ppm):8.18(d,4H,J=7.72Hz),7.93-7.97(m,16H),7.72(d,8H,J=6.88Hz),7.50-7.54(m,16H),7.39-7.42(m,14H),7.31-7.34(m,10H),7.16(t,8H,J=7.52Hz),6.90(d,4H,J=8.36Hz),5.70(d,4H,J=8.32Hz),4.17(br,4H),3.67(br,8H).31P NMR(CDCl3,ppm):30.4(t,4P,JP-P=31.5Hz),22.7(m,2P,JP-P=25.0Hz),4.2(t,2P,JP-P=25.1Hz,JPt-P=2676Hz).HRMS(ESI):根据C118H96Au3ClN2P8Pt[M-2ClO4]2+的计算值:1305.1880;实测值:1305.1839.IR(KBr,cm-1):2107w(C≡C),1100s(ClO4-).
实施例2:配合物2的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-C6H4But-4)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2,产率:72%。1H NMR(CDCl3,ppm):7.89-7.93(m,8H),7.74-7.77(m,8H,7.66-7.70(m,8H),7.49-7.52(m,14H),7.31-7.34(m,14H),7.02-7.05(m,8H,6.54(d,4H,J=8.04Hz),5.41(d,4H,J=8.04Hz),4.08(br,4H),3.85(br,4H),3.54(br,4H)0.98-1.2(m,18H).31P NMR(CDCl3,ppm):29.1(t,4P,JP-P=32.6Hz),17.8(m,2P,JP-P=30.0Hz),4.8(t,2P,JP-P=27.1Hz,JPt-P=2694Hz).HRMS(ESI):根据C102H98Au3ClN2P8Pt[M-2ClO4]2+计算值:1196.1927;实测值:1196.1976.IR(KBr,cm-1):2105w(C≡C),1100s(ClO4-).
实施例3:配合物3的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-2-PhCarb-9)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):8.01-8.03(m,8H),7.74-7.77(m,10H),7.66-7.69(m,10H),7.51-7.55(m,12H),7.43-7.49(m,12H),7.37-7.41(m,16H),6.95(m,10H),6.78(d,2H,J=8.4Hz),6.02(s,2H),5.78(d,2H,J=8.4Hz),4.13(br,4H),4.03(br,4H),3.65(br,4H).31P NMR(CDCl3,ppm):29.6(t,4P,JP-P=32.0Hz),18.1(m,2P,JP-P=30.6Hz),6.2(t,2P,JP-P=30.0Hz,JPt-P=2726Hz).HRMS(ESI):根据C118H96Au3ClN2P8Pt[M-2ClO4]2+的计算值:1305.1880;实测值:1305.1909.IR(KBr,cm-1):2099w(C≡C),1100s(ClO4-).
实施例4:配合物4的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-3-CarbC6H4Carb-9)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:55%。1H NMR(CDCl3,ppm):8.23(d,4H,J=7.56Hz),8.04-8.07(m,8H),7.87-7.90(m,6H),7.76-7.81(m,18H),7.58-7.61(m,10H),7.48-7.52(m,14H),7.42-7.47(m,20H),7.02-7.05(m,10H),6.95(d,4H,J=8.48Hz),6.05(s,2H),5.91(d,2H,J=8.52Hz),4.16(br,4H),4.06(br,4H),3.68(br,4H).31P NMR(CDCl3,ppm):29.7(t,4P,JP-P=32.5Hz),18.2(m,2P,JP-P=30.6Hz),6.2(t,2P,JP-P=27.4Hz,JPt-P=2706Hz).HRMS(ESI):根据C142H110Au3ClN4P8Pt[M-2ClO4]2+的计算值:1470.7458;实测值:1470.7484.IR(KBr,cm-1):2104w(C≡C),1100s(ClO4-).
实施例5:配合物5的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-3-PTZ-10-Et)替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):7.87-7.89(m,8H),7.74-7.77(m,8H),7.66-7.69(m,8H),7.48-7.51(m,12H),7.36-7.39(m,12H),7.12-7.15(m,16H),6.95(t,2H,J=7.20Hz),6.86(d,2H,J=8.16Hz),6.18(d,2H,J=8.52Hz),5.35(d,2H,J=8.38Hz),5.04(s,2H),4.04(br,4H),3.93(br,4H),3.84(q,4H,J=6.90Hz),3.54(br,4H),1.41(t,6H,J=6.84Hz).31P NMR(CDCl3,ppm):29.6(t,4P,JP-P=32.0Hz),18.4(m,2P,JP-P=29.4Hz),5.8(t,2P,JP-P=29.0Hz,JPt-P=2706Hz).HRMS(ESI):根据C110H96Au3ClN2P8PtS2[M-2ClO4]2+的计算值:1289.1600;实测值:1289.1571.IR(KBr,cm-1):2099w(C≡C),1100s(ClO4-).
实施例6:配合物6的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-4-C6H4NPh2)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):7.89-7.91(m,16H),7.61-7.66(m,8H),7.49-7.51(m,12H),7.29-7.32(m,12H),7.29-7.32(m,8H),7.20(t,4H,J=7.4Hz),7.05-7.09(m,12H),7.02(d,8H,J=7.4Hz),6.36(d,4H,J=8.8Hz),5.40(d,4H,J=8.0Hz),4.05(br,4H),3.56(br,4H),3.51(br,4H).31P NMR(CDCl3,ppm):30.4(t,4P,JP-P=31.6Hz),22.5(m,2P,JP-P=31.4Hz),3.7(t,2P,JP-P=29.9Hz,JPt-P=2696Hz).HRMS(ESI):根据C118H100Au3ClN2P8Pt[M-2ClO4]2+的计算值:1307.2036;实测值:1307.2065.IR(KBr,cm-1):2096w(C≡C),1100s(ClO4-).
实施例7:配合物7的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-4-C6H4-phenim)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):8.87(d,2H,J=8.0Hz),8.80(d,2H,J=8.4Hz),8.74(d,2H,J=8.4Hz),7.86-7.91(m,6H),7.83-7.84(m,10H),7.68-7.72(m,8H),7.59-7.61(m,12H),7.51-7.56(m,22H),7.43-7.46(m,2H),7.30-7.36(m,12H),7.13(d,2H,J=8.0Hz),7.04(t,6H,J=7.2Hz),6.96(d,4H,J=8.0Hz),5.33(d,4H,J=8.0Hz),4.06(br,4H),3.57(br,4H),3.48(br,4H).31P NMR(CDCl3,ppm):30.4(t,4P,JP-P=31.4Hz),22.7(m,2P,JP-P=31.4Hz),4.1(t,2P,JP-P=30.1Hz,JPt-P=2670Hz).HRMS(ESI):根据C136H106Au3ClN4P8Pt[M-2ClO4]2+的计算值:1432.2302;实测值:1432.2273.IR(KBr,cm-1):2101w(C≡C),1100s(ClO4-).
实施例8:配合物8的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-4-C6H4-2-benzimd-1-Ph)2替代Pt(PPh3)2(C≡C-4-C6H4Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):7.89-7.91(m,8H),7.80-7.82(m,10H),7.57-7.61(m,12H),7.45-7.49(m,18H),7.34-7.36(m,6H),7.26-7.29(m,20H),6.99(t,6H,J=7.2Hz),6.94(d,4H,J=8.4Hz),5.30(d,4H,J=8.4Hz),4.07(br,4H),3.54(br,4H),3.46(br,4H).31P NMR(CDCl3,ppm):30.4(t,4P,JP-P=31.4Hz),22.6(m,2P,JP-P=30.6Hz),3.9(t,2P,JP-P=29.8Hz,JPt-P=2686Hz).HRMS(ESI):根据C120H98Au3ClN4P8Pt[M-2ClO4]2+的计算值:1332.1989;实测值:1332.2010.IR(KBr,cm-1):2092w(C≡C),1100s(ClO4-).
实施例9:配合物9的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-4-C6H4-2-benzimd-1-Ph)(C≡C-3-Carb-9-Ph)替代Pt(PPh3)2(C≡C-4-C6H4-Carb-9)2。产率:70%。1H NMR(CDCl3,ppm):8.02-8.06(m,4H),7.80-7.82(m,16H),7.65-7.69(m,8H),7.51-7.55(m,10H),7.39-7.42(m,20H),7.24-7.26(m,4H),7.04-7.06(m,4H),6.93-6.95(m,4H),6.72(d,1H,J=8.4Hz),6.01(s,1H),5.70(d,1H,J=8.0Hz),5.42(d,2H,J=8.0Hz),4.04(br,4H),3.86(br,4H),3.69(br,4H).31P NMR(CDCl3,ppm):29.4(t,4P,JP-P=31.4Hz),17.9(m,2P,JP-P=31.4Hz),5.5(t,2P,JP-P=30.4Hz,JPt-P=2686Hz).HRMS(ESI):根据C119H97Au3ClN3P8Pt[M-2ClO4]2+的计算值:1318.6934;实测值:1318.6961.IR(KBr,cm-1):2104w(C≡C),1100s(ClO4-).
实施例10:配合物10的制备
制备方法与实施例1中方法相同,仅是使用Ag(tht)ClO4替代Au(tht)Cl。产率:76%.1H NMR(CDCl3,ppm):8.20(d,4H,J=7.72Hz),7.87-7.91(m,8H),7.69-7.72(m,14H),7.48-7.51(m,10H),7.35-7.38(m,10H),7.29-7.33(m,18H),7.20-7.23(m,12H),6.66(t,4H,J=6.44Hz),5.19(d,4H,J=8.32Hz),4.17(br,4H),3.46(br,8H).31P NMR(CDCl3,ppm):19.3(m,2P,JPt-P=2402Hz),9.6(m,1P,JP-P=37.2Hz),6.3(m,1P,JP-P=37.2Hz),-0.6(m,4P).HRMS(ESI):根据C118H96Ag3ClN2P8Pt[M-2ClO4]2+的计算值:1172.0958;实测值:1172.0993.IR(KBr,cm-1):2084w(C≡C),1098s(ClO4-).
实施例11:配合物11的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡CC6H4But-4)2和Ag(tht)ClO4替代Pt(PPh3)2(C≡C-4-C6H4-Carb-9)2和Au(tht)Cl。产率:84%.1H NMR(CDCl3,ppm):7.74-7.78(m,14H),7.53-7.56(m,10H,7.43-7.46(m,4H),7.29-7.33(m,14H),7.18-7.21(m,10H),7.09-7.12(m,8H,6.20(d,4H,J=8.08Hz),4.91(d,4H,J=8.04Hz),3.96(br,4H),3.31(br,4H),3.10(br,4H)0.96-1.2(m,18H).31P NMR(CDCl3,ppm):19.1(m,2P,JP-P=27.9Hz,JPt-P=2344Hz),9.0(m,1P,JP-P=37.8Hz),5.7(m,1P,JP-P=37.8Hz),-4.0(m,4P).IR(KBr,cm-1):2082w(C≡C),1098s(ClO4-).
实施例12:配合物12的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-2-Carb-9-Et)2和Ag(tht)ClO4替代Pt(PPh3)2(C≡C-4-C6H4-Carb-9)2和Au(tht)Cl。产率:75%。1H NMR(CDCl3,ppm):7.81-7.84(m,8H),7.72-7.75(m,6H),7.64-7.67(m,8H),7.37-7.40(m,6H),7.38-7.41(m,6H),7.32-7.36(m,12H),7.24-7.27(m,6H),7.19-7.22(m,12H),7.07-7.10(m,10H),6.32(d,2H,J=8.52Hz),5.96(s,2H),5.11(d,2H,J=8.12Hz),4.29(q,4H,J=7.16Hz),4.25(br,4H),3.45(br,4H),3.29(br,4H),1.43(t,6H,J=7.12Hz).31P NMR(CDCl3,ppm):18.9(m,2P,JP-P=28.1Hz,JPt-P=2406Hz),9.3(m,1P,JP-P=37.3Hz),5.8(m,1P,JP-P=37.3Hz),-0.8(m,2P,JP-P=30.8Hz),-3.6(m,2P,JP-P=30.8Hz).HRMS(ESI):根据C110H96Ag3ClN2P8Pt[M-2ClO4]2+的计算值:1124.0958;实测值:1124.0975.IR(KBr,cm-1):2071w(C≡C),1098s(ClO4-).
实施例13:配合物13的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-3-CarbC6H4Carb-9)2和Ag(tht)ClO4替代Pt(PPh3)2(C≡C-4-C6H4-Carb-9)2和Au(tht)Cl。产率:72%.1H NMR(CDCl3,ppm):8.24(d,2H,J=7.72Hz),7.91-7.94(m,12H),7.73-7.78(m,18H),7.62-7.65(m,4H),7.51-7.54(m,8H),7.40-7.44(m,8H),7.31-7.35(m,16H),7.24-7.27(m,14H),7.13-7.16(m,10H),6.47(d,2H,J=8.60Hz),6.05(s,2H),5.15(d,2H,J=7.76Hz),4.28(br,4H),3.48(br,4H),3.33(br,4H).31P NMR(CDCl3,ppm):18.9(m,2P,JP-P=27.2Hz,JPt-P=2302Hz),9.3(m,2P,JP-P=37.6Hz),3.4(m,4P,JP-P=28.2Hz).HRMS(ESI):根据C142H110Ag3ClN4P8Pt[M-2ClO4]2+的计算值:1337.1536;实测值:1337.1550.IR(KBr,cm-1):2071w(C≡C),1098s(ClO4-).
实施例14:配合物14的制备
制备方法与实施例1中方法相同,仅是使用Pt(PPh3)2(C≡C-3-PTZ-10-Et)和Ag(tht)ClO4替代Pt(PPh3)2(C≡C-4-C6H4-Carb-9)2和Au(tht)Cl。产率:78%。1H NMR(CDCl3,ppm):8.05(d,2H,J=7.76Hz),7.91-7.94(m,8H),7.72-7.76(m,6H),7.54-7.57(m,8H),7.38-7.42(m,10H),7.23-7.28(m,20H),7.13-7.16(m,6H),7.01-7.04(m,10H),5.58(s,2H),5.05(d,2H,J=8.12Hz),4.23(br,4H),3.39(q,4H,J=6.92Hz),3.23(br,8H),1.05(t,6H,J=7.16Hz).31P NMR(CDCl3,ppm):18.0(m,2P,JP-P=26.4Hz,JPt-P=2336Hz),9.1(m,1P,JP-P=31.4Hz),5.6(m,1P,JP-P=31.4Hz),-1.5(m,2P),-4.4(m,2P).HRMS(ESI):根据C110H96Ag3ClN2P8PtS2[M-2ClO4]2+的计算值:1156.0678;实测值:1156.0700.IR(KBr,cm-1):2092w(C≡C),1096s(ClO4-).
实施例15:光致发光性能测试
在Edinburgh FLS920荧光光谱仪上分别测试实施例1-14中制备的配合物1-14在二氯甲烷溶液、固体粉末及48.5%mCP:48.5%OXD-7(1:1):3%本发明配合物(重量比)薄膜中的激发光谱、发射光谱、发光寿命和发光量子产率。利用直径为142mm的积分球测定固体粉末样品的发光量子产率。
PtAu3配合物1-9和PtAg3配合物10-14的磷光发射波长(λem)、发光寿命(τem)和量子产率(ΦPL)列于表1。
表1.PtM3配合物1-14的光致发光性能数据
[a]掺杂薄膜包含重量比为48.5%的mCP,48.5%的OXD-7和3%的PtM3配合物。
由表1结果可知,PtAu3配合物1-9在二氯甲烷溶液和固体状态具有中等强度的光致发光,在48.5%的mCP,48.5%的OXD-7和3%的PtM3配合物的掺杂薄膜中则具有非常强的磷光,发光量子产率高达76.8%-90.5%,是有机发光二极管很理想的发光材料。而PtAg3配合物10-14具有光致发光性能,也可以用于有机发光二极管中。
实施例16:有机发光二极管制备与电致发光性能测试
分别利用实施例3、4、5、8、9中制备的磷光配合物3、4、5、8或9为发光材料,以3%的重量百分比掺杂到mCP(48.5%):OXD-7(48.5%)混合主体材料中作为发光层制备有机发光二极管,器件结构为:ITO/PEDOT:PSS(50nm)/48.5%mCP:48.5%OXD-7:3%本发明配合物3、4、5、8或9(50nm)/BmPyPb(50nm)/LiF(1nm)/Al(100nm)。
首先分别利用去离子水、丙酮、异丙醇清洗ITO基底,再采用UV-臭氧处理15分钟。将过滤后的PEDOT:PSS水溶液在旋涂仪上以4800转/分钟的转速旋涂到ITO基底上,在140℃干燥20分钟后得到50nm厚度的空穴注入层。其次利用旋涂仪将过滤后的浓度为5.5mg/mL的48.5%mCP:48.5%OXD-7:3%本发明配合物3、4、5、8或9(重量百分比)的二氯甲烷溶液以2100转/分钟的转速旋涂到PEDOT:PSS薄膜上形成50nm厚度的发光层。随后,将ITO基底置于真空度不低于4×10-4Pa的真空腔中,依次热蒸镀厚度为50nm的Bmpypb、1nm厚的LiF电子注入层、以及100nm厚度的Al为器件阴极。
发光二极管器件性能测试在室温干燥的空气环境(湿度<30%)中进行。电致发光性能参数包括电致发光波长(λEL),启亮电压(Von),最大亮度(Lmax),最大电流效率(CEmax),最大功率效率(PEmax)和最大外量子效率(EQEmax)。相关电致发光数据列于表2。
表2.基于磷光配合物3、4、5、8或9的有机发光二极管性能数据
[a]亮度为1cd/m2的启亮电压.[b]最大亮度.[c]最大电流效率.[d]最大功率效率.[e]最大外量子效率.[f]色度坐标。
由表2结果可知,利用配合物3、4、5、8或9作为发光材料,运用溶液旋涂制备的有机发光二极管具有优秀的电致发光性能,器件最大发光亮度超过10000cd/m2,最大电流效率为38.7到62.8cd/A,最大外量子效率(EQE)超过10%。
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
一种磷光PtM3异四核配合物及其制备方法和用途专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0