专利摘要
本发明提供了一种多取代稠合苯并呋喃类衍生物及其制备方法,与现有技术相比,本发明提供了一系列新的多取代稠合苯并呋喃类衍生物。相对于普通多取代稠合苯并呋喃类衍生物,本发明制备的多取代稠合苯并呋喃类衍生物有多环的存在,其结构更加复杂多样,在化工生产、临床医药中也将表现出更加广阔的用途前景。并且,本发明提供的制备方法简便、高效,反应时间短,效率高。
说明书
技术领域
本发明属于有机化合物领域,具体涉及一种多取代稠合苯并呋喃类衍生物及其制备方法。
背景技术
苯并呋喃类化合物因其广泛的药理活性以及它们在自然界的广泛存在而引起人们的注意。比如,从丹参、百部、野茉莉等植物中提取出来的2-芳基取代的苯并呋喃类化合物具有良好的生理活性,如抗病毒、抗肿瘤、抗菌、抗自由基、抗氧化作用等,常用于选择性腺苷A1受体拮抗剂、免疫抑制剂等。
最近又发现官能化的单或二苯并呋喃类衍生物还可以作为蓝光发光材料应用于OLED中,而Jung等也对含有苯并呋喃单体的有机染料聚合物在太阳能电池中的应用进行了研究;Romagnoli等合成了一系列2-(3,4,5-三甲氧基苯甲酰基)-苯并呋喃衍生物,发现这类化合物在抑制癌细胞的生长方面具有潜在的活性。
Yue等在2005年从邻碘代茴香醚出发,先与端基炔发生Sonogashira偶联,后在I2,PhSeCl,或者p-O2NC6H4SCl的存在下发生亲电子环化作用,以较高的收率生成2,3-二取代苯并呋喃环,如附图1所示。Cho等在此基础上采用并行合成法对苯并呋喃类化合物进行了库合成,成功得到了121种多取代的苯并呋喃化合物。
Carril等以水做溶剂,使烷基(或芳基)苄基酮衍生物在CuI-TMEDA的催化下生成相应的苯并呋喃化合物,如图2所示。
Sanz等从苄基-2-卤代苯醚出发,用3当量的t-BuLi处理形成有机锂中间体,然后再与羧酸酯反应,再经酸化或者脱水就得到相应的2-芳基-3-取代苯并呋喃衍生物,如图3所示。
Sanz等从间卤代氨基甲酰酯出发,用NaH或n-BuLi处理后接着与相应的亲电试剂反应,得到o-2(F,Cl)-3-卤代苯氨基甲酰酯,经水解、Sonogashira偶联及关环反应得到4-卤代苯并呋喃衍生物,如图4所示,4-位的卤素很容易转化为其他的官能团,而4-位官能化基团取代的苯并呋喃化合物用其他的方法是不易得到的。
综上所述欲完成此类反应需苛刻的反应条件、强碱的作用及配体的存在。
发明内容
为解决上述技术问题,本发明提供了一种多取代稠合苯并呋喃类衍生物的制备方法,简便、高效,反应时间短,效率高。
本发明还提供了一种多取代稠合苯并呋喃类衍生物,具有多环存在,结构更复杂,有广阔的应用前景。
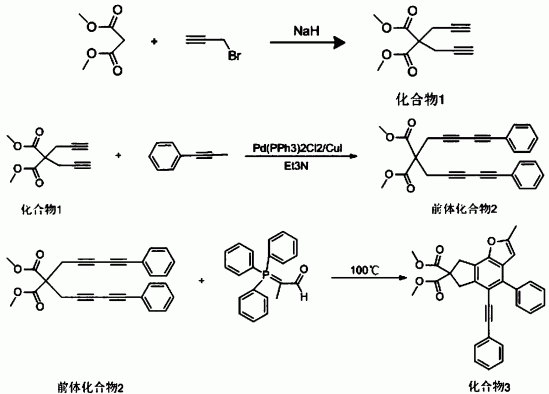
本发明提供的一种多取代稠合苯并呋喃类衍生物的制备方法,包括以下步骤:
(1)以氢化钠为催化剂,将丙二酸酯与炔丙基溴加入到无水乙腈中冰水浴,反应,然后纯化分离,得到白色固体化合物1;
(2)将化合物1与苯乙炔基溴或取代的苯乙炔基溴混合在Pd(PPh3)2Cl2/CuI的无水无氧催化体系中,以三乙胺作碱,以无水乙腈为溶剂,室温下搅拌反应,纯化分离后得到产物,即前体化合物2;
(3)在95-100℃的条件下,步骤(2)所制备的前体化合物2在甲苯溶剂中与2-(三苯基正膦基)丙醛反应,自然冷却至室温停止反应;将产物纯化分离,得到白色固体,即多取代稠合苯并呋喃类衍生物。
进一步的,步骤(1)中氢化钠、丙二酸酯、炔丙基溴与无水乙腈的摩尔比为4-5:1:2.2-3.2:20-23;所述丙二酸酯为丙二酸二甲酯。
步骤(1)的反应温度在0-5℃;反应时间在5小时以上;
步骤(1)中所述纯化分离具体为:产物加水洗涤,用乙酸乙酯萃取,减压旋干,得到黄棕色固体产物,即化合物1。
步骤(2)中所述化合物1与苯乙炔基溴或取代的苯乙炔基溴、Pd(PPh3)2Cl2/CuI、三乙胺和无水乙腈的物质的量比为1:2.2-3.2:0.03-0.04:4-5:30-45;步骤(2)所述搅拌反应,时间在10小时以上。
步骤(2)中所述洗涤分离具体为:产物用水洗涤,用乙酸乙酯萃取,减压旋干,用体积比为1:60的乙酸乙酯:石油醚柱层析分离,得到浅黄色固体产物,即前体化合物2。
步骤(2)中所述Pd(PPh3)2Cl2/CuI的无水无氧催化体系中,摩尔比Pd(PPh3)2Cl2:CuI=3:1。
步骤(3)中前体化合物2、2-(三苯基正膦基)丙醛与甲苯的摩尔比为1.2-1.5:1:28-66;
步骤(3)中所述反应,是指100-105℃反应8-9小时;
步骤(3)中所述纯化分离具体为:将所得产物用水洗涤,乙酸乙酯萃取,减压旋干,用体积比1:40的乙酸乙酯:石油醚的柱层析分离,得到白色固体,即多取代稠合苯并呋喃类衍生物,即化合物3,柱层析产率约为77.8%。
本发明所制备的多取代稠合苯并呋喃类衍生物,结构式为:
其中E1和E2相同,为CO2R,R为直链烷基、支链烷基、饱和烃类、不饱和烃类或芳香烃类基团;R1为卤素、直链烷基、支链烷基、酯基、烷氧基以及其相应的衍生物。
进一步的,所述R为甲基,R1为氢,其结构式为::
与现有技术相比,本发明提供的制备方法从新的角度,利用witting试剂涉及甲基的迁移电子的转移等反应过程在无催化剂的条件下简便、高效地合成了苯并呋喃类衍生物,且反应时间短,效率高。并且,提供了一系列新的多取代稠合苯并呋喃类衍生物。相对于普通多取代稠合苯并呋喃类衍生物,本发明制备的多取代稠合苯并呋喃类衍生物有多环的存在,其结构更加复杂多样,在化工生产、临床医药中也将表现出更加广阔的用途前景。
附图说明
图1为Yue等在2005年从邻碘代茴香醚出发制备2,3-二取代苯并呋喃环的反应方程式;
图2为Carril等利用烷基(或芳基)苄基酮衍生物在CuI-TMEDA的催化下生成相应的苯并呋喃化合物的方程式;
图3为Sanz等从苄基-2-卤代苯醚出发制备2-芳基-3-取代苯并呋喃衍生物的方程式;
图4为Sanz等从间卤代氨基甲酰酯出发得到4-卤代苯并呋喃衍生物的方程式;
图5为多取代稠合苯并呋喃类衍生物的结构式;
图6为实施例1制备的多取代稠合苯并呋喃类衍生物的结构式;
图7为实施例1制备的多取代稠合苯并呋喃类衍生物的核磁共振氢谱;
图8为实施例1制备的多取代稠合苯并呋喃类衍生物的核磁共振碳谱;
图9为实施例1制备的多取代稠合苯并呋喃类衍生物的反应过程。
具体实施方式
实施例1
一种多取代稠合苯并呋喃类衍生物,其结构式为:
一种多取代稠合苯并呋喃类衍生物的制备方法,包括以下步骤:
(1)以830mmol氢化钠为催化剂,将200mmol丙二酸二甲酯与440mmol炔丙基溴加入到210mL无水乙腈中冰水浴,搅拌反应8小时,产物加水洗涤,用乙酸乙酯萃取,减压旋干,得到棕黄色固体产物,即化合物1;
(2)将80mmol化合物1与200mmol苯乙炔基溴混合在Pd(PPh3)2Cl2/CuI(2.56mmol/0.85mmol)的无水无氧催化体系中,摩尔比Pd(PPh3)2Cl2:CuI=3:1,以336mmol三乙胺作碱,以150mL无水乙腈为溶剂,室温下搅拌反应12小时,产物用水洗涤,用乙酸乙酯萃取,减压旋干,用体积比为1:60的乙酸乙酯:石油醚柱层析分离,得到浅黄色固体产物,即前体化合物2。
(3)在100℃的条件下,步骤(2)所制备的1.2mmol前体化合物2在5mL甲苯溶剂与1mmol 2-(三苯基正膦基)丙醛反应18小时,得化合物3,即多取代稠合苯并呋喃类衍生物的粗产物;将制备的多取代稠合苯并呋喃类衍生物的粗产物用水洗涤,乙酸乙酯萃取,减压旋干,用体积比乙酸乙酯:石油醚=1:40柱层析分离,得到白色固体产物,即多取代稠合苯并呋喃类衍生物,柱层析产率约为77.8%。
所制备的多取代稠合苯并呋喃类衍生物结构通过;1H NMR;13C NMR来测定。
白色固体产物:
1H NMR(300MHz,CDCl3)δ7.64-7.25(m,10H),6.31(s,1H),3.92-3.89(d,2H),3.80(s,6H),2.42(s,3H).
13C NMR(125MHz,CDCl3)δ172.53,156.09,150.67,139.77,138.83,135.99,131.65,130.41,128.69,128.59,128.26,127.81,124.16,121.19,112.73,103.24,94.59,87.98,60.33,53.42,42.00,38.21,14.32。
一种多取代稠合苯并呋喃类衍生物及其制备方法专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0