专利摘要
本发明属于发光材料技术领域,具体涉及配合物Eu(L)(DMA)2(NO3)及其合成方法。本发明要解决的技术问题是提供一种红色发光材料。本发明的技术方案是配合物Eu(L)(DMA)2(NO3),分子结构如下:本发明还提供了配合物Eu(L)(DMA)2(NO3)的合成方法。本发明的配合物为发光材料领域提供了新选择。
权利要求
1.配合物Eu(L)(DMA)2(NO3),分子结构如下:
2.如权利要求1所述的配合物,其特征在于:由硝酸铕、配体H2L出发制备而成,所述配体是一种含O的多齿配体,配体中的羧基O与中心原子Eu配位形成如下结构的九配位金属-有机配合物。
3.配合物Eu(L)(DMA)2(NO3)的合成方法,其特征在于:包括如下步骤:采用溶剂热合成方法,按下列摩尔配比称取原料:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=13~17︰18~22︰5198~5631︰11858~12846,混合物搅拌0.5~3h,最后于密闭容器中在75~85°C下反应3~5天;自然冷却后,过滤,得到无色块状晶体即为目标产物。
4.如权利要求3所述的合成方法,其特征在于:H2L︰Eu(NO3)3·6H2O︰DMA︰CH3OH的摩尔比为15︰20︰5414︰12445。
5.如权利要求3或4所述的合成方法,其特征在于:所述的密闭容器为反应釜。
6.如权利要求3~5任一项所述的合成方法,其特征在于:所述的反应时间为4天。
7.如权利要求3~6任一项所述的合成方法,其特征在于:所述的反应温度为80℃。
8.如权利要求3~7任一项所述的合成方法,其特征在于:所述的无色块状晶体依次用水、甲醇洗涤,自然干燥。
说明书
技术领域
本发明属于发光材料技术领域,具体涉及配合物Eu(L)(DMA)2(NO3)及其合成方法。
背景技术
稀土配合物的发光性能早在1942年由Weissmantl发现,他利用不同的β-二酮类铕(Ⅲ)配合物吸收紫外光后,出现了铕(Ⅲ)离子的特征线状发射,自此人们开始接触到稀土配合物的光致发光现象。到60至70年代初,为了寻找激光的工作物质,才开始对稀土光致发光配合物进行了系统的研究,大量关于稀土配合物光致发光性质的研究在不同领域内展开。到目前为止,稀土配合物的发光性能一直受到人们的广泛研究,尤其是对铕配合物的研究,Eu3+因其荧光寿命长,激发态具有较强的荧光发射,在发光分子器件、荧光成像、癌症辐射治疗、荧光标记、荧光分析等方面的广泛应用已成为人们关注的热点。因此设计和开发铕配合物成为红光材料研究的重点之一。
一直以来铕配合物的发光机理是光致发光配合物研究的热点之一。一般认为稀土铕配合物的荧光主要是配体吸收紫外光后发生π→π*跃迁,电子由基态跃迁到激发态,将受激能量传递给中心离子Eu3+,中心离子发出特征荧光,这种通过配体敏化中心离子发光的效应称为天线效应。
由此可见,影响铕配合物发光的因素有以下3点:配体的光吸收强度;配体→铕离子的能量传递效率和铕离子本身的发射效率。所以,对于铕配合物来说可以通过选择合适的配体来提高发光强度。
鉴于苯乙烯基或亚苯乙烯基(-C6H4CH=CH-)是典型共轭发色基团,延伸的离域π电子体系,可提高配体对紫外光的吸收并有利于能量传输到中心Eu离子,使其发出特征光。所以苯乙烯基型有机配体与Eu离子形成的稀土配合物是一类独特的光致发光材料。
以往报道的稀土铕配合物发光材料,主要存在配体选择方面的不足,选用非芳香类羧酸配体,共轭程度低,光吸收能力低,不利于能量向中心铕离子传输,使发光性能受阻。在铕中心来源选择方面也存在不足,以往报道稀土铕配合物都选用氧化铕作为铕的来源,这样导致铕离子与配体的配位能力降低。
发明内容
本发明要解决的技术问题是提供一种红色发光材料。
本发明的技术方案是配合物Eu(L)(DMA)2(NO3),分子结构如下:
其中所述的配合物是由硝酸铕、配体H2L出发制备而成,所述配体是一种含O的多齿配体,配体中的羧基O与中心原子Eu配位形成如下结构的九配位金属-有机配合物。
本发明还提供了配合物Eu(L)(DMA)2(NO3)的合成方法,包括如下步骤:采用溶剂热合成方法,按下列摩尔配比称取原料:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=13~17︰18~22︰5198~5631︰11858~12846,混合物搅拌0.5~3h,最后于密闭容器中在75~85°C下反应3~5天;自然冷却后,过滤,得到无色块状晶体即为目标产物。
优选的,H2L︰Eu(NO3)3·6H2O︰DMA︰CH3OH的摩尔比为15︰20︰5414︰12445。
优选的,所述的密闭容器为反应釜。
优选的,所述的反应时间为4天。
优选的,所述的反应温度为80℃。
优选的,所述的无色块状晶体依次用水、甲醇洗涤,自然干燥。
本发明的有益效果:
本发明所选用的配体,含有苯乙烯基这样的共轭基团,形成大π键,有利于配体对紫外光的吸收,配体→铕离子的能量传递效率高,上述优点有利于配体敏化铕离子,致使铕离子发特征红光。配体中含有多齿氧配位基,选用硝酸铕作为铕离子的来源,有利于氧原子与中心离子铕配位,形成一种新型红色发光材料,有较好潜在的应用前景和基础研究意义。此稀土铕配合物既具备小分子有机化合物易提纯和高荧光量子效率的优点,而且通常具有更高的热稳定性,200℃开始分解(图4),为新型荧光发光材料发展铺垫了更加优越的条件。本发明方法操作简单,产率可达到50.4%~63.0%。
附图说明
图1H2L的结构式
图2Eu(L)(DMA)2(NO3)的单晶结构图
图3晶体发红光(在365nm紫外灯照射下)
图4配合物的热重图
图5配合物的固体荧光光谱(最大发射波长在730nm,最大激发波长在430nm)
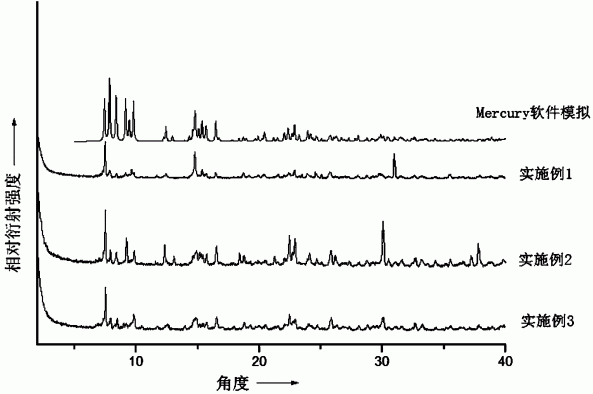
图6x-射线粉末衍射
具体实施方式
配合物的不对称单元中包含一个去质子的L2-配体,一个铕离子,一个硝酸根离子,两个DMA分子。铕离子采用九配位方式,与两个螯合的双齿羧基、两个桥连得羧基、一个螯合的硝酸根、两个来自两个不同的DMA分子的氧原子配位。配体H2L一端的羧基氧原子以桥连的方式连接到两个铕离子上,另一端的羧基氧原子通过螯合/桥连的方式配位到两个铕离子上。该材料经荧光实验后,发现在730nm处有非常强的荧光发射(见图3、5),成为一种新的红色发光材料,有较好潜在的应用前景和较好的基础研究意义。
本发明中所使用的H2L的制备过程参考文献[1]。
本发明所选用的配体H2L共轭程度非常大。在反应过程中H2L脱去了两个H原子,变成L2-与硝酸铕中的铕离子配位。得到的产品以H2L为依据计算产率。即根据反应物中H2L与Eu(L)(DMA)2(NO3)的摩尔比,换算得到理论上应得到的Eu(L)(DMA)2(NO3)质量,再根据实际得到的Eu(L)(DMA)2(NO3)质量,后者占前者的比值即为产率。
本发明中对最终产物进行x-射线衍射分析,得到其晶体结构。并对最终产物进行一系列表征,如元素分析、红外,荧光、x-射线粉末衍射。
实施例1本发明配合物的制备
按下列摩尔配比称取原料:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=13︰18︰5198︰11858,置于50mL玻璃烧杯中,混合物搅拌0.5h,然后转移入25mL反应釜中,在75℃下反应3天后,自然冷却至室温,观察到无色晶体,即目标产品,将其从母液中过滤出来,依次用水、甲醇洗涤,完后自然干燥。
产品Eu(L)(DMA)2(NO3)中的C、H、N元素进行元素分析,计算值(%):C,46.88;H,4.98;N,5.47。实际测得(%):C,48.01;H,5.07;N,5.40。FT-IR(KBr,cm-1):2063(m),1660(m),1480(m),1380(m),1246(m),983(m)。说明:元素分析值由Perkin-Elmer2400元素分析仪测得;红外光谱由NicoletImpact410FTIR光谱仪以KBr为底在400~4000cm-1范围内测得。
对得到的目标产物进行x-射线衍射分析,获得其晶体结构(见图2)。证明了该配合物每个铕离子采用九配位方式,配体H2L一端的羧基氧原子以桥连的方式连接到两个铕离子上,另一端的羧基氧原子通过螯合/桥连的方式配位到两个铕离子上。
对目标产物用RF-5301PC荧光仪测得产品在730nm处有最大发射(在430nm最大激发下);结果表明此发明产品是一种红光发光材料(见图5)。用岛津XRD-6100型x-射线衍射仪进行粉末衍射测试,测试图谱的峰与经Mercury软件模拟的图谱的峰能很好的匹配,说明此晶体即为目标产物,且样品纯度较高(见图6)。
将本实施例重复多次,实际生产得到Eu(L)(DMA)2(NO3)的质量保持在50.8~62.3mg,计算得到为产率50.8%~62.3%。
实施例2本发明配合物的制备
按下列摩尔配比称取原料:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=15︰20︰5414︰12445,置于50mL玻璃烧杯中,混合物搅拌2h,然后转移入25mL反应釜中,在80℃下反应4天后,自然冷却至室温,观察到无色晶体,即目标产品,将其从母液中过滤出来,依次用水、甲醇洗涤,完后自然干燥。
对产物进行元素分析、红外、荧光、x-射线粉末衍射表征,得到数据与实施例1相似。说明用实施例2制得的晶体结构未发生变化且产品较纯(见图6),性能也为发生变化(见图5)。
将本实施例重复多次,根据实际生产得到Eu(L)(DMA)2(NO3)的质量60.5~72.6mg,计算得到产率为52.5%~63.0%。
实施例3本发明配合物的制备
按下列摩尔配比称取原料:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=17︰22︰5631︰12846,置于50mL玻璃烧杯中,混合物搅拌3h,然后转移入25mL反应釜中,在85℃下反应5天后,自然冷却至室温,观察到淡黄色晶体,即目标产品,将其从母液中过滤出来,依次用水、甲醇洗涤,完后自然干燥。
对产物进行元素分析、红外、荧光、x-射线粉末衍射表征,得到数据与实施例1相似。说明用实施例3制得的晶体,结构也没有发生变化且产品较纯(见图6),性能也未发生变化(见图5)。
将本实施例重复多次,根据实际生产得到Eu(L)(DMA)2(NO3)的质量65.9mg~78.2mg,计算得到产率为50.4%~59.8%。
由图5和图6可知,制得铕配合物Eu(L)(DMA)2(NO3),所称取原料摩尔配比为:H2L︰Eu(NO3)3·6H2O︰DMA(N,N-二甲基乙酰胺)︰CH3OH(甲醇)=13~17︰18~22︰5198~5631︰11858~12846较为适宜,反应时间为3-5天较为适宜;所得的铕配合物Eu(L)(DMA)2(NO3)较纯,荧光最大发射波长在730nm处(在430nm波长激发下),说明此配合物发较强的红光,有可能成为新型的荧光发光材料。
参考文献:
[1]Koepp,E.; F.Perkin-Synthesemit Synthesis.1987,(2),177-178.。
配合物Eu(L)(DMA) 2 (NO 3 )及其合成方法专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0