专利摘要
本发明的目的在于提供一种新型单聚物及其制造方法,该单聚物具有适合与其它单聚物共聚合的聚合特性,并可获得优良的光透性及热稳定性;灵敏度、分辨率不损失及耐干腐蚀抗腐蚀剂性能、与有机溶剂的溶解性优良、线性边缘粗糙度小;并提供一种形成方法,该方法适合远紫外光准分子激光器光刻及电子线光刻等的抗蚀剂组成物,以及用该抗蚀剂组成物的图谱(样品)。
权利要求
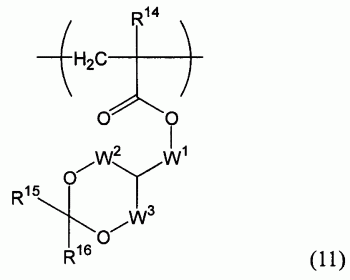
1.通式(11)如下所示
其中,W1表示直接结合1~6碳的亚甲链,
W2表示直接结合1~3碳的亚甲链,
W3表示1~3碳的亚甲链,
R14表示氢原子和甲基,
R15表示4~16碳的桥连环烃和含有4~16碳的桥连环烃的1~6碳的直链或分支烷基,
R16表示氢原子和1~6碳的直链或分支烷基,
R15和R16相结合可以形成4~16碳的桥连环烃,
所述1~6碳的亚甲链可含有1~3碳的烷基,其中可有一个以上的醚键,所述1~3碳的亚甲链可含有羰基,所述烷基、桥连环烃可含有1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上组成单位的聚合体。
2.通式(12)如下所示
其中,W4表示直接结合1~6碳的亚甲链,
R17表示氢原子和甲基,
R18、R19可相同或不同,指氢原子和1~6碳的直链或分支烷基,4~16碳的环烃和含有4~16碳的环烃的1~6碳的直链或分支烷基,
R18和R19相结合可以形成4~16碳的桥连环烃,
所述亚甲链可含有1~3碳的烷基,其中可含有一个以上的醚键,所述烷基、环烃可含1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的烷氧基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上组成单位的聚合体。
3.通式(13)如下所示
其中,W5表示直接结合1~6碳的亚甲链,
W6表示直接结合1~3碳的亚甲链,
W7表示1~3碳的亚甲链,
R20指氢原子和甲基,
R21、R22可相同或不同,指氢原子和1~6碳的直链或分支烷基、4~16碳的环烃和含有4~16碳的环烃的1~6碳的直链或分支烷基,
R21和R22相结合可以形成4~16碳的环烃,
所述1~6碳的亚甲链为可含有1~3碳的烷基,其中可含有一个以上的醚键,所述1~3碳的亚甲链可含有羰基,所述烷基、环烃为含1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的烷氧基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上为下述通式(8)~(10)中所表示的单位中选择1种以上组成单位的聚合体,
其中,R8表示氢原子和甲基,
R9表示1~6碳的直链或分支烷基、4~8碳的环烃、4~16碳的桥连环烃,
所述烷基、环烃、桥连环烃是含有1~6碳的直链或分支烷基,还可以含有羟基、羧基和1~6碳的醇和被酯化的羧基;
其中,R10表示氢原子和甲基,
R11表示氢原子、亲水官能团和含有亲水官能团的1~6碳的直链或分支烷基、4~8碳的环烃,4~16碳的桥连环烃,
所述烷基、环烃、桥连环烃或亲水官能团的1~6碳的直链或分支烷基,还可以含有羟基、羧基和1~6碳的醇和被酯化的羧基;
其中,q表示1~4的整数,
R12、R13表示各种氢原子、甲基和乙基。
4.如权利要求3所述通式(13)所表示的聚合体,其特征在于所述聚合体的单位为权利要求1和权利要求2中所述的通式(11)和通式(12)中所表示的单位。
5.如权利要求1~4中任意一项所述聚合体,其特征在于平均分子量为1,000~100,000。
6.将至少一种如权利要求1~5所述聚合体与所述通式(8)~(10)中表示的单位中所选的一种以上组成单位所含聚合体中的至少一种以上进行混合,形成聚合体混合物。
7.从上述通式(13)所表示的单位选择一种以上组成单位的聚合体,当中至少有一种含有抗蚀组成物。
8.如权利要求1~5中任意一项所述聚合体或如权利要求6中所述聚合混合物,其特征在于所述聚合体和所述混合物为抗蚀组成物。
9.一种抗蚀组成物,其特征在于含有如权利要求1~5中任意一项所述聚合体或如权利要求6中所述聚合混合物和光氧发生剂。
10.将如权利要求7~9所述的抗蚀组成物涂抹在被加工基板上,在波长小于250nm的光或电子射线下,进行曝光工程即成型方法。
11.权利要求10所述成型方法中曝光工程使用的光为ArF受激准分子激光器所产生的光。
12.将如权利要求7~9所述抗蚀组成物涂抹在被加工基板上,在波长小于250nm的光或电子射线下进行曝光工程,如有必要,使用现象液也包括在成型方法中。
说明书
技术领域技术领域
本发明涉及一种采用桥连环烃和含有桥连环烃的烷基中所含的5-亚甲-1,3-二噁茂烷-4-酮衍生物作为涂料、粘合剂、油墨用树脂、防腐材料等树脂构成成分的原料及其制造方法,以及防腐用途中重要的聚合体,特别涉及一种使用受激准分子激光器或电子射线进行细微加工时所适用的防腐用聚合体,以及使用此聚合体的抗蚀组成物及其形成方法。
技术背景背景技术
现有技术中已经存在下述通式(14)所表示的5-亚甲-1,3-二噁茂烷-4-酮衍生物及其制造方法。
其中,R23、R24可相同或不同,为氢、烷基、可有取代基的芳基、环己基,
R23和R24结合的碳原子形成苯基,也可形成(CH2)m的环构造,
所述芳基的取代基为1~12碳的直链或分支烷基或卤原子,m为2以上的整数。
例如:J.Organic Chemical(1992),57(12),3380-7、TetrahedronLett.(1989),30(52),7305-8中提到上述技术。其中所述公式(14)中的R23为氢原子、R24为t-丁基,所述化合物是利用β-(苯硫酚)甲基乳酸与酮或醛进行反应经由5-(苯硫)甲基-1,3-二噁茂烷-4-酮衍生物进行展开而制成的。但是,若采用5-(苯硫)甲基-1,3-二噁茂烷-4-酮衍生物的方法,需要在-78℃下,用3-卤氯过安息香酸氧化5-(苯硫)甲基-1,3-二噁茂烷-4-酮衍生物之后,再用三乙磷酸盐进行处理,工作非常复杂。
特开平7-70106号公报上,公开了R24为取代或未取代的烷基的化合物,特开平10-316609号公报上,公开了R23及R24为烷基的化合物。这些文献上记载了采用乳酸与酮或醛进行反应制备5-甲基-1,3-二噁茂烷-4-酮衍生物的方法,即四盐化碳或环己烷酸为溶媒的条件下采用5-位溴化剂使N-溴亚胺溴化,得到5-溴-5-甲基-1,3-二噁茂烷-4-酮衍生物,然用盐基进行脱溴化氢反应的方法。
SU606313号公报上记载了,所述通式(14)中R23、R24为氢原子和R23、R24为(CH2)m的环构造(m为2以上的整数)时的化合物;Polym.Prepr.(Am.Chemical Society,Div.Polym.Chemical)(1987),28(1),154-5中披露了所述通式(14)中R23和R24为甲基时的化合物;特开平3-37214号公报上记载了所述通式(14)中R23和R24为氢原子、1~12碳的烷基和以卤原子为取代基的1~12碳的烷基时的化合物。这些文献上记载了采用β-卤乳酸与醛进行反应,合成5-卤甲基-1,3-二噁茂烷-4-酮衍生物,然后用胺等盐基进行脱溴化氢的反应的制备公式(14)所述化合物的方法。
但是,没有报导披露以桥连环烃做为取代基的5-亚甲-1,3-二噁茂烷-4-酮衍生物的制造方法。
此外,已有将含有5-亚甲-1,3-二噁茂烷-4-酮衍生物的单体重合的聚合体作为水溶性聚合物和生分解性聚合物的报道。例如:T.Endo et al,Macromol.Chem.Phys.Vol.202,1602-1605(2001)记载了2,2-甲基-5-亚甲-1,3-二噁茂烷-4-酮衍生物与甲基丙息烯酸甲的共聚合体;Chin.J.Polym.Sci.Vol.10,350-355(1992)中记载了2-5-亚甲-1,3-二噁茂烷-4-酮衍生物的聚合体。但是,没有报导披露以桥连环烃做为取代基的5-亚甲-1,3-二噁茂烷-4-酮衍生物的聚合体。
另外,以光刻术的发展为背景,为实现素子的高密度化、高集中化,在精加工的领域里的半导体晶体和液晶晶体的制造高速的向细微化推进。作为细微化的手法,一般将曝光的光的短波长化,即将传统以g线(波长:438nm)、i线(波长:365nm)为代表的紫外线转化为远紫外线即曝光光源。
现在,KrF受激准分子激光(波长:248nm)光刻技术的市场导入,以及即将被导入的ArF受激准分子激光(波长:193nm)光刻技术,甚至,作为次世代技术,正在研制中的F2受激准分子激光(波长:157nm)光刻技术。以及正在被全力研制中的在形式上稍有不同的光刻技术和电子射线光刻技术。
所以,IBM公司倡导“化学增幅型抗蚀物”,现在正在全力地针对短波长的光和电子射线的抗蚀物进行改良和开发。
因此,随着光的短波长化,抗蚀物所使用的树脂的构造也产生了变化。例如:针对于KrF受激准分子激光光刻技术的波长为248nm的光,采用以酸解离性的溶解抑制基保护的高透明的氢氧基。但ArF受激准分子激光光刻技术的波长为193nm的光的情况下,上述树脂由于透光性不够,很多场合不能使用。
因此,针对于ArF受激准分子激光光刻技术的波长为193nm的光的抗蚀树脂,透明的丙烯基系列树脂及环烯烃系列树脂受到关注。特开平4-39665号公报、特开平10-207069号公报、特开平9-090637号公报中记载了丙烯基系列树脂。特开平10-153864号公报中记载了环烯烃系列树脂。
另外,作为针对于ArF受激准分子激光光刻技术所使用的抗蚀树脂,甲基丙烯酸2-甲基-2-金刚烷的共聚合体倍受注目。此共聚合体在S.Takechi et al,Journal of Photopolymer Science andTechnology,Vol.9,No.3,475-487(1996)和特开平9-73173号公报中均有记载。所述共聚合体2-甲基-2-金刚烷在酸的作用下裂解得到高耐干腐蚀、高敏感度及高清晰度的性质。但,这种共聚合体由于恐水性高,现象液不易涂抹。
为了降低恐水性,导入含内脂构造的甲基丙烯酸的共聚合体,以及脂环式构造的氢氧基等亲水性基。例如:特开平10-319595号公报、特开平10-274852号公报记载了脂内含金刚烷的丙烯基酸的共聚合体,特开2002-82441号公报记载了含内脂的环烯烃或丙烯基系列的共聚合体。
但是,所述丙烯基系列树脂、环烯基系列树脂在与抗蚀物溶液调制时,由于溶解性不足,会导致溶解时间长甚至不溶,使抗蚀溶液的调制很困难。此外,所述丙烯基系列树脂、环烯烃系列树脂的耐热性不足,在使用所述丙烯基系列树脂及环烯烃系列树脂时,在接受激准分子激光光刻技术的处理后,会出现抗蚀物型局部杂疵,发生线路障碍,回路不均及短路等现象,引起了对半导体制造工业的担心。
发明内容发明内容
本发明的目的在于提供一种透光性与热稳定性优越的独立聚合体或共同聚合体及其制造方法。即无损抗蚀物、敏感度、清晰度、耐腐性及对有机溶液的溶解性优越、线路障碍少的聚合体,和适合于远紫外线受激准分子激光光刻技术、电子射线光刻技术的抗蚀物及这种抗蚀物形成方法。
为达到上述目的,本发明的发明者们的研究所得的含有桥连环烃和含桥连环烃的烷基的5-亚甲-1,3-二噁茂烷-4-酮衍生物的聚合体及共同聚合体,有其优越的透光性、热稳定性及对有机溶液的溶解性。是一种线路障碍少,适合于远紫外线受激准分子激光光刻技术、电子射线光刻技术的抗蚀物。
本发明的第一项发明内容为下述通式(11)所示
其中,W1表示直接结合1~6碳的亚甲链,
W2表示直接结合1~3碳的亚甲链,
W3表示1~3碳的亚甲链,
R14表示氢原子和甲基,
R15表示4~16碳的桥连环烃和含有4~16碳的桥连环烃的1~6碳的直链或分支烷基,
R16表示氢原子和1~6碳的直链或分支烷基,
R15和R16相结合可以形成4~16碳的桥连环烃,
所述1~6碳的亚甲链可含有1~3碳的烷基,其中可有一个以上的醚键,所述1~3碳的亚甲链可含有羰基,所述烷基、桥连环烃可含有1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上组成单位的聚合体。
本发明的第二项发明内容为下述通式(12)所示
其中,W4表示直接结合1~6碳的亚甲链,
R17表示氢原子和甲基,
R18、R19可相同或不同,指氢原子和1~6碳的直链或分支烷基,4~16碳的环烃和含有4~16碳的环烃的1~6碳的直链或分支烷基,
R18和R19相结合可以形成4~16碳的桥连环烃,
所述亚甲链可含有1~3碳的烷基,其中可含有一个以上的醚键,所述烷基、环烃可含1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的烷氧基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上组成单位的聚合体。
本发明的第三项发明内容为下述通式(13)所示
其中,W5表示直接结合1~6碳的亚甲链,
W6表示直接结合1~3碳的亚甲链,
W7表示1~3碳的亚甲链,
R20指氢原子和甲基,
R21、R22可相同或不同,指氢原子和1~6碳的直链或分支烷基、4~16碳的环烃和含有4~16碳的环烃的1~6碳的直链或分支烷基,
R21和R22相结合可以形成4~16碳的环烃,
所述1~6碳的亚甲链为可含有1~3碳的烷基,其中可含有一个以上的醚键,所述1~3碳的亚甲链可含有羰基,所述烷基、环烃为含1~6碳的直链或分支烷基,还可以含有羟基、羧基、2~6碳的酰基和1~6碳的烷氧基和1~6碳的醇和被酯化的羧基,
从所表示的单位中选择1种以上为下述通式(8)~(10)中所表示的单位中选择1种以上组成单位的聚合体。
其中,R8表示氢原子和甲基,
R9表示1~6碳的直链或分支烷基、4~8碳的环烃、4~16碳的桥连环烃,
所述烷基、环烃、桥连环烃是含有1~6碳的直链或分支烷基,还可以含有羟基、羧基和1~6碳的醇和被酯化的羧基;
其中,R10表示氢原子和甲基,
R11表示氢原子、亲水官能团和含有亲水官能团的1~6碳的直链或分支烷基、4~8碳的环烃,4~16碳的桥连环烃,
所述烷基、环烃、桥连环烃或亲水官能团的1~6碳的直链或分支烷基,还可以含有羟基、羧基和1~6碳的醇和被酯化的羧基;
其中,q表示1~4的整数,
R12、R13表示各种氢原子、甲基和乙基。
所述通式(13)所表示的聚合体的单位为通式(11)和通式(12)中所表示的单位。
上述聚合体的平均分子量为1,000~100,000。
本发明的第四项发明内容为上述聚合体与所述通式(8)~(10)中表示的单位中所选的一种以上组成单位所含聚合体中的至少一种以上进行混合,形成聚合体混合物。
本发明的第五项发明内容为从上述通式(13)所表示的单位选择一种以上组成单位的聚合体,当中至少有一种含有抗蚀组成物。
本发明的第六项发明内容为上述聚合体或上述聚合混合物为抗蚀组成物。
本发明的第七项发明内容为一种抗蚀组成物,含有如上述聚合体或如上述聚合混合物和光氧发生剂。
本发明的第八项发明内容为将如上述的抗蚀组成物涂抹在被加工基板上,在波长小于250nm的光或电子射线下,进行曝光工程即成型方法。
上述成型方法中曝光工程使用的光为ArF受激准分子激光器所产生的光。
本发明的第九项发明内容为将如上述抗蚀组成物涂抹在被加工基板上,在波长小于250nm的光或电子射线下进行曝光工程,如有必要,使用现象液也包括在成型方法中。
附图说明附图说明
图1表示式(19)所示化合物的1H-NMR光谱(270MHz,CDCl3),并且
图2表示式(19)所示化合物的13C-NMR光谱(270MHz,CDCl3);
图3表示式(21)所示化合物的1H-NMR光谱(270MHz,CDCl3),并且
图4表示式(21)所示化合物的13C-NMR光谱(270MHz,CDCl3);以及
图5表示式(23)所示化合物的1H-NMR光谱(270MHz,CDCl3),并且
图6表示式(23)所示化合物的13C-NMR光谱(270MHz,CDCl3)。
具体实施方式具体实施例
以下是本发明的详细说明
本发明中的桥连环烃是以金刚烷和原菠烷为代表的。下述通式(15)
其中,A1、B1可相同或不同,表示直链或分支亚烷基。
下述通式(16)表示含有构造的取代基
其中,A2、B2可相同或不同,表示直链或分支亚烷基。
本发明的下述通式(1)
其中,R1表示4~16碳的桥连环烃和含4~16碳的桥连环烃的1~6碳直链或分支烷基,
R2表示氢原子和1~6碳直链或分支烷基,
R1和R2相结合可以形成4~16碳的桥连环烃,
所述烷基、所述桥连环烃可以是1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。所述5-亚甲-1,3-二噁茂烷-4-酮衍生物的R1可以是:2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚壬基等桥连环烃。
其中,抗蚀组成物在使用时,若需要强的耐干腐蚀性,最好采用2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基,若从重合物的透光性及Tg等的热稳定性出发,最好采用1-金刚烷基、2-原菠烷基。
上述通式(1)所表示的R2可以是:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基等。其中若考虑较佳的抗蚀组成物的涂抹性最好采用甲基和乙基。此外,上述通式中的R1和R2相结合的碳原子与桥连环烃所形成的衍生物可以是:螺旋〔原菠烷基-2,2’-(5’-亚甲-1’,3’-二噁茂烷-4’-酮衍生物)〕、螺旋〔金刚烷基-2,2’-(5’-亚甲-1’,3’-二噁茂烷-4’-酮衍生物)〕。
上述构造最好为:5-亚甲-2-(1-金刚烷基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-原菠烷基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(1-金刚烷甲基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷甲基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(1-金刚烷乙基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷乙基)-2-甲基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(1-金刚烷基)-2-乙基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷基)-2-乙基-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-乙基-2-(2-原菠烷基)-1,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(1-金刚烷甲基)-2-乙基-1-,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷甲基)-2-乙基-1-,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(1-金刚烷乙基)-2-乙基-1-,3-二噁茂烷-4-酮衍生物、5-亚甲-2-(2-金刚烷乙基)-2-乙基-1-,3-二噁茂烷-4-酮衍生物等。
上述的构造是1~6碳的直链或分支烷基,甚至是羟基、羧基、氨基、硝基、磺酸基、酰胺基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。所述基中,同样的基可含有2个以上。抗蚀物就透光性而言,最好为1~6碳的直链或分支烷基、羟基、羧基、碳数2~6的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基,抗蚀物材料就基板附着性而言,最好为羟基、羟甲基,羟乙基。并且可含有2个以上同样的基。
下述通式(2)作为上述通式(1)中衍生物的中间体
其中,X表示氯原子和溴原子,
R1和R2与所述通式(1)相同。
所述的5-卤-5-甲基-1,3-二噁茂烷-4-酮衍生物的R1、R2与上述通式(1)的所举例相同。另外,溴原子的存在使上述通式(2)中的衍生物与上述通式中的酮衍生物的变换反应得以顺利进行。
下述通式(3)为上述通式(2)中的衍生物
其中,R1和R2与公式(1)相同。
所述的5-甲基-1,3-二噁茂烷-4-酮衍生物作为原料加入卤化剂进行反应,5位的卤化制成。
上述通式(3)中的衍生物的R1、R2与公式(1)所举例相同。
下述通式(17)为公式(3)的导通衍生物
其中,R1和R2与公式(1)相同。
其中酮和醛可由已知的制法合成。比如,通式(17)中的化合物与乳酸的脂可同时进行脱水和脱乙醇的反应,此反应的副反应为20℃~环流温度中,酮和醛或某种乳酸进行过剩反应。乳酸的酸性足可使反应进行,如添加路易氏酸更佳。
上述通式(17)中的化合物作为二甲体、烯醇醚体与蚁酸反应后,可伴有乳酸的脱甲醇反应。在20℃~环流温度中,二甲体与乳酸反应,二甲体、烯醇醚体以乳酸的过剩条件为好。乳酸的酸性足可使反应进行,如添加路易氏酸更佳。
这些反应如使用倾析器,脱水、脱乙醇的效果更好。也可使用光学活性乳酸。
上述通式(3)中衍生物的卤化反应中,作为通式(2)所述衍生物制造过程的卤化剂为:N-氯琥珀酸亚胺、1,3-二氯-5,5-二甲海因、酸盐甲烷、N-溴琥珀酸亚胺、1,3-二溴-5,5-二甲海因、酸盐甲烷、溴等。其中,就反应性、卤化位置的选择讲,N-溴琥珀酸亚胺为佳。
通式(3)中制备通式(2)中衍生物的卤化反应中的卤化剂的用量为通式(3)中衍生物的0.1~10倍(摩尔倍数)。若使卤化剂效率高一些,卤化剂的使用量应答于通式(3)中的衍生物使用量的0.5倍(摩尔倍数)。此外,卤化剂用量的多少是为了防止分解反应,则其用量应小于衍生物用量的2倍(摩尔倍数),其中1.5倍(摩尔倍数)为最佳。
已往的卤化反应中,会使用如偶氮二异丁晴等的原子团发生剂,然而,在本发明中不使用原子团发生剂也可使反应顺利进行。如使用,发生剂用量小于衍生物用量的0.1倍(摩尔倍数),如想减少夹杂物,使用量可在0.01倍(摩尔倍数)。
此卤化反应可使用现有机溶解液,如:戊烷、乙烷、庚烷、环戊烷、环乙烷、乙醚、二异丙醚、甲基-tert-丁基醚、四氢呋喃、四盐化碳、三氯甲烷、盐化亚甲等。其中,乙烷、庚烷、环乙烷、四盐化碳为佳。
为使反应顺利进行,有机溶解液的用量为公式(3)中的衍生物的0.1倍(质量倍数)以上为好,0.5以上更好,质量倍数为1时最佳。有机溶解液的使用量从反应速度角度出发,以公式(3)中的衍生物的质量倍数为100以下为好,50以下更好,质量倍数为20以下时最佳。
有机溶解液中可含水,但含水量越少越好。
本发明的反应,应在密闭容器中,减压、常压、加压均可,温度在沸点以下,生成物放置在冷却器中冷却。反应温度通常为50℃~65℃,以55℃~60℃之间为宜。
通常,使用卤化剂进行的卤化反应导致原子团的形成,原子团的形成反应是在80℃左右。在此温度下,原料与卤化物进行明显的分解反应,上述通式(2)中的衍生物的收效大幅减少,此分解反应为含桥连环烃的取代基贴付于2位时即使在65℃以下也反应明显。但是,本发明者们发现,在此温度下,卤化反应存在不进行反应的情况。
反应时间根据反应温度而决定,以1~48小时为宜。
根据本发明所进行的卤化反应制造出公式(2)中的衍生物。本反应中由于很好的抑制了副反应而得到的衍生物,可直接进行脱卤化氢的反应,并且,在反应液中清除了未反应的卤化物(如N-溴琥珀酸亚胺)及副生成物(如琥珀酸亚胺)后,可进行脱卤化氢反应。如有必要,也可除去溶解液或更换容器。也可用一些普遍的柱色谱或减压蒸镏等方法进行提纯。
另外,通式(2)中的衍生物的R1和R2不同时,2-位的碳原子成为光学异性体的不整碳。这些光学异性体,用已知的优先晶析法、光学分割柱等光学分割法进行分离。这些光学异性体的(R)-体、(S)-体或混合体可进行脱卤化氢的反应。
上述通式(1)所表示的衍生物的制造方法为通式(2)中的衍生物即下述通式(5)
其中,R3、R4、R5可相同或不同,表示氢、1~4碳的直链或分支烷基。
所表示的酰胺化合物、进行脱卤化氢反应。
公式(1)中的衍生物为下述通式(4)
其中,X表示氯原子和溴原子,
R1和R2与公式(1)相同。
所述的5-卤甲基-1,3-二噁茂烷-4-酮衍生物与在上述通式(5)中的酰胺化合物进行脱卤化氢反应。
通式(4)中的衍生物的R1、R2作为很好的示例与公式(1)中的同时被列举。另外,由于溴原子的存在使公式(4)中的衍生物的X与公式(1)中的衍生物变换时反应也可顺利进行。
上述通式(4)中的衍生物作为公式(17)中酮和醛的原料,可以是用已知的制法合成的β-溴乳酸、β-氯乳酸的β-卤乳酸等脂。此时的温度为20℃~环流温度,其中β-卤乳酸等的脂及酮和醛适宜过剩条件。
所述的酮和醛与蚁酸反应制得二甲体、烯醇醚体之后,与β-卤乳酸反应可得通式(4)中所述化合物。此时的温度为20℃~环流温度,二甲体、烯醇醚体与β-卤乳酸适宜过剩的条件。
上述通式(4)中的化合物在进行合成反应时,可添加路易氏酸,如使用β-卤乳酸时,β-卤乳酸的酸性足够使反应进行。此反适宜在密闭的容器中、沸点以下,减压、常压、加压均可进行。挥发的原料及生成物放置在冷却器中进行冷却。利用倾析器等进行除水。
通式(4)中的化合物的合成反应中可使用β-卤乳酸、酮和醛及消旋混合物。这时的化合物的原料可为一般的光学活性体或消旋混合物。另外,当公式(4)中化合物的R1、R2不同时,2-位的碳原子成为不整碳,由于光学异性体的存在,有可能成为消旋混合物。此消旋混合物可用优先晶析法、光学分割柱等光学分割法分离。
本发明的通式(5)所述酰胺化合物的R5、R6、R7可以是:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基等。通式(4)的酮衍生物如采用N-甲基甲酰胺、N-乙基甲酰胺、N,N-二甲基甲酰胺、N,N-二乙基甲酰胺等均能使反应顺利进行,其中采用N-二甲基甲酰胺效果更好。
上述通式(1)中可得出化合物,但现有技术中采用脱卤化反应,反应中会明显阻碍分解反应、反应液着色、生成物结晶化,并且还会发生生成物收效低下、精制困难等问题。
以前的脱卤反应时使用的氢化锂、氢化钠、甲醇钠、乙醇钠、钠-t-丁氧、烷氧基、羧酸盐、三甲胺、三乙胺、三辛胺、氮苯、三甲基吡啶、1,5-二氮环〔4.3.0〕-5-壬烯、1,8-二氮环〔5.4.0〕-7-十一碳烯、1,4-二氮环〔2.2.2〕辛烷等盐酸类在通式(2)、通式(5)中的衍生物的脱卤化氢反应时,会出现分解反应,就不能得到通式(1)所述的衍生物。
本发明所述制造方法中,可以解决通式(2)、通式(4)中使用酰胺化合物的酮衍生物,进行脱卤化氢反应中的问题。通式(5)中的酰胺化合物的盐基性非常弱,一般不作为脱卤化氢反应试剂,但在本发明的化合物中可有效的进行脱卤化氢反应。
上述的盐基与通式(5)中的酰胺化合物并用时,上述的盐基的分解可得到抑制,但还会阻碍反应液着色、生成物结晶化以及使反应后的精制变得困难。
上述通式(5)中的酰胺化合物使用量为通式(2)、(4)中的衍生物的0.1~100倍(摩尔倍数)。通式(5)中的酰胺化合物的使用量从效果角度出发为通式(2)、(4)中的衍生物的0.5倍(摩尔倍数)以上为好,1倍(摩尔倍数)以上更好,5倍(摩尔倍数)为最佳。另外,通式(5)中的酰胺化合使用量从反应后废液处理的角度考虑,以通式(2)、(4)中的衍生物的50倍(摩尔倍数)以下为宜,30倍以下更好。本发明的有机溶解液可以是:戊烷、乙烷、庚烷、辛烷、异辛烷、环戊烷、环乙烷、苯、甲苯等碳化氢系列溶解液;甲醇、乙醇、n-丙醇、异丙醇、n-丁醇、sec-丁醇、t-丁醇、异丁醇、n-胺醇、异胺醇、n-己醇、n-庚醇、n-辛醇、n-壬醇、n-癸醇、十二烷醇、十六烷醇、十八烷醇、苄醇、三苯基甲醇、乙二醇、1,2-丙二醇,1,4-丁二醇,甲酚、二甲苯酚、等醇系列的溶解液;二乙甲醚、二乙乙醚、三乙甲醚、三乙乙醚、三氢呋喃、乙醚、甲基-tert-丁基醚、二异丙醚等醚系列溶解液;四盐化碳、三氯甲烷、盐化亚甲等含氯系列溶解液。
其中,戊烷、乙烷、庚烷、辛烷、异辛烷、环戊烷、环乙烷、苯烷、甲苯、二异丙醚、甲基-tert-丁基醚等溶解度低,适合通式(5)中的酰胺化合物。低溶解度液溶解通式(5)中的酰胺化合物,反应后,可回收通式(1)所述衍生物。如不使用溶解液进行脱卤化氢反应,可采用低溶解度的溶解液将通式(1)中衍生物抽出。这些溶解液中含少量通式(5)所述的酰胺化合物,容易用水洗去。而且,如不使用溶解液反应后,也可用水将生成物洗净。
有机溶解液的使用量从反应速度和废溶解液量的角度考虑,通式(2)、(4)中的衍生物的质量倍数为100倍以下为好,50倍以下更好,质量倍数为20倍以下为最佳。
本发明的反应可以在密闭容器中,减压、常压、加压中均可进行,温度在沸点以下,挥发的原料及生成物放置在冷却器中进行冷却环流。
反应温度通常为-30℃~120℃,从反应速度的角度考虑,反应温度以0℃以上为宜,10℃以上更好。另外,从抑制分解的角度考虑,反应温度以60℃以下为宜,40℃以下更好。已往的脱卤化氢反应,由于反应生热的原因,要边冷却边添加盐基。然而,采用本发明通式(5)所述的酰胺化合物,发热量少,无高温分解反应,所以没有冷却的必要。
反应时间由反应温度决定,但通常以1~48小时为宜。
本发明进行脱卤化氢反应时,如有必要可在反应液中添加防止重合剂。关于防止重合剂没有具体规定,可以是:对苯二酚、甲氧对苯二酚、对苯醌、p-tert-对特丁基邻苯二酚等苯醌系列防止重合剂;2,6-2-tert-丁苯酚、2,4-2-tert-丁苯酚、2-tert-丁基-4、6-二甲苯、2,6-2-tert-丁基-4-甲苯酚、2,4,6-3-tert-丁苯酚等苯酚系列防止重合剂;二苯胺、N,N’-二苯-p-对苯二胺、夹硫氮蒽等胺系列防止重合剂;二甲氨荒酸铜、二乙氨荒酸铜、二丁氨荒酸铜等氨荒酸铜系列防止重合剂。防止重合剂可为一种或者两种以上并用。添加量以上述通式(2)、(4)中的衍生物的5%(质量比)以下为佳,1%(质量比)以下更好,0.1%(质量比)以下最佳。根据本发明的制造方法,进行脱卤化氢反应可制造出通式(1)中的衍生物。在本反应中,由于很好的抑制了副反应,可通过简单的操作过程制造出高纯度的通式(1)所述的衍生物。精制方法可使用公认的再结晶、用水或有机溶解液冲洗、溶解分别法、柱色谱、蒸馏等方法。
另外,当通式(1)中衍生物的R1和R2不同时,2-位的碳原子成为光学异性体的不整碳。这些光学异性体,用已知的优先晶析法、光学分割柱等光学分割法进行分离。这些光学异性体(R)-体、(S)-体或混合体可作为涂料、粘和剂、油墨用树脂、抗蚀物等的构成成分树脂的原料单体使用。
而且,本发明的透光性、热稳定性优越的单体聚合体及共同聚合体具有敏感度、清晰度高、耐干腐蚀性强及不损害抗蚀性能,对于有机溶解液的溶解性好、线路障碍少等特点,适合于采用远紫外线受激准分子激光光刻技术、电子射线光刻技术的抗蚀物以及这种抗蚀物形成方法。
本发明的聚合体的第一项为下述通式(6)
其中,R1、R2表示与通式(1)同样的取代基,
从所表示的单位中选择一种或二种以上构成聚合体。
此聚合体是将通式(1)中的化合物重合得到的。只把通式(1)中的单体重合、共同重合或与通式(1)中的单体以外的单体共同重合均可。
本发明的聚合体的第二项为下述通式(11)
其中,W1表示直接结合1~6碳的亚甲链,
W2表示直接结合1~3碳的亚甲链,
W3表示1~3碳的亚甲链,
R14表示氢原子和甲基,
R15表示4~16碳的桥连环烃或含4~16碳的桥连环烃的1~6碳的直链或分支烷基,
R16表示氢原子或1~6碳的直链或分支烷基,
R15与R16相结合形成4~16碳的桥连环烃。
所述1~6碳的亚甲链可含1~3碳烷基,所述1~3碳的亚甲链中可含有羧基,还可含有所述烷基、桥连环烃、1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。
从所表示的单位中选择一种构成聚合体。
上述通式(11)中作为W1的示例直接结合(指与W1相邻的氧及碳原子直接结合)CH2、CH2CH2、CH2CH2CH2、CH(CH3)CH2、CH2O、CH2CH2O、CH2CH(CH3)O、CH(CH3)CH2O、CH2CH2OCH2CH2O、CH2CH(CH3)OCH2CH(CH3)O、CH(CH3)CH2OCH(CH3)CH2O等。W1可含有1~3碳的烷基作为取代基,并可含有一个以上的醚键。从聚合体保持安定的角度出发,W1与CH2、CH2CH2O、CH2CH(CH3)O直接结合为宜。
作为W2的示例直接结合(指与W2相邻的氧及碳原子直接结合)CH2、C(O)、CH2CH2、CH2C(O)、CH2CH2CH2、CH2C(O)CH2等。从聚合体保持安定的角度出发直接结合(指与W2相邻的氧及碳原子直接结合)CH2、C(O)、CH2C(O)为宜。
作为W3的示例可以是CH2、C(O)、CH2CH2、CH2C(O)、CH2CH2CH2、CH2C(O)CH2等,从聚合体保持安定的角度出发,以CH2、C(O)、CH2C(O)。
上述通式(11)中的化合物R15的示例为2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基等。同样的基可采用两个以上。
这些基中,使用抗蚀物时,耐干腐蚀性优越的为:2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基。重合物的透光性及Tg等的热稳定性优越的为:1-金刚烷基、2-原菠烷基。
上述通式(11)中的化合物R16的示例为:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基等。其中,使用抗蚀物时,涂抹性优越的为甲基及乙基。
上述通式(11)中的化合物R15与R16结合在一起的碳原子即形成的桥连环烃为金刚烷基与原菠烷基等。
上述构造中可为含1~6碳的烷基,甚至含有羟基、羧基、胺基、亚硝酸根、砜基、酰胺、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。这些基中同样的可有二个以上。这些基中,使用抗蚀物时,透光性优越的为:1~6碳的直链或分支烷基、羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。耐干腐蚀性强的为甲基、乙基。这些基中,使用抗蚀物时,对于基板的附着性优越的为:羟基、羟甲基、羟乙基。这些基中同样的可有二个以上。
此聚合体为下述通式(18)
其中,W1~3、R14~16与通式(11)中相同。
从所表示的单体中选择一种以上进行重合。使通式(18)中的单体重合或共同重合。也可与通式(18)中的单体以外的单体共同重合。
上述通式(18)的单体的示例为下述通式(I-1)~(I-45)所表示的单体
(I-1) (I-2) (I-3)
(I-4) (I-5) (I-6)
(I-7) (I-8) (I-9)
(I-10) (I-11) (I-12)
(I-13) (I-14) (I-15)
其中,R14与(11)相同。
(I-16) (I-17) (I-18)
(I-19) (I-20) (I-21)
(I-22) (I-23) (I-24)
(I-25) (I-26) (I-27)
(I-28) (I-29) (I-30)
其中,R14通式(11)相同。
(I-31) (I-32) (I-33)
(I-34) (I-35) (I-36)
(I-37) (I-38) (I-39)
(I-40) (I-41) (I-42)
(I-43) (I-44) (I-45)
其中,R14通式(11)相同。
其中,聚合体的安定性的保持以(I-37)~(I-45)为好。作为上述单体的一例按下述通式可以制造
(方案1)
2-金刚烷基、1-金刚烷甲酮、降莰烷及酮衍生物的原料酮可在市面购买或使用已知的制法合成。
酸性条件下,从酮与羟基羧可得出已众所周知。反应溶解液以甲苯、环乙烷、乙烷等低溶解性溶解液为宜,为提高收效应除水。乙醇的脂化反应,可在通常的脂化条件下进行。作为反应剂可采用(甲)丙烯基酸卤化物、(甲)丙烯基酸无水物、(甲)丙烯基酸脂及(甲)丙烯基酸等,也可用酸、盐基、路易氏酸等。
上述反应的生成物中含有多种构造异性体、几何异性体、光学异性体。在本发明中,即使含有异性体的混合物或中间体也可使用。如有必要,可使用通常的蒸馏、再结晶或光柱谱等方法进行精制。
本发明的聚合体为下述通式(12)
其中,W4表示直接结合1~6碳的亚甲链,
R17表示氢原子和甲基,
R18、R19可相同或不同,表示氢原子和1~6碳的直链或分支烷基,4~16碳的环烃和含4~16碳的环烃的1~6碳的直链或分支烷基,
所述亚甲链可含1~3碳的烷基,其中可含有一个以上的醚键,所述烷基,环烃可含1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基和1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。
从所表示的单位中选择1种以上构成单位的聚合体。
上述通式(12)中W4的示例是:直接结合(指与W1相邻的氧及碳原子直接结合)CH2、CH2CH2、CH2CH2CH2、CH(CH3)CH2、CH2O、CH2CH2O、CH2CH(CH3)O、CH(CH3)CH2O、CH2CH2OCH2CH2O、CH2CH(CH3)OCH2CH(CH3)O、CH(CH3)CH2OCH(CH3)CH2O等。(CH2)a可含有1~3碳的烷基的取代基和一个以上的醚键。从聚合体的安定性保持角度出发,W4直接结合以CH2、CH2CH2O、CH2CH(CH3)O为好。
再有,作为R18、R19的示例可以是:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基、环戊基、环己基、环庚基、2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基等。上述通式(12)中的化合物R18与R19结合在一起的碳原子即形成的桥连环烃为金刚烷基与原菠烷基等。
在使用抗蚀物时,耐干腐蚀性优越的为:2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基等4~16碳的桥连环烃或含4~16碳的桥连环烃的1~6碳的直链或分支烷基。R19以氢原子、1~6碳的直链或分支烷基为好。其中,R18以2-原菠烷基、1-金刚烷基为好,R19以甲基或乙基为好。
另外,R18、R19结合在一起的碳原子共同形成金刚烷基与原菠烷基。
以上的构造中可含1~6碳的烷基,甚至含有羟基、羧基、胺基、亚硝酸根、砜基、酰胺、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。这些基中同样的可有二个以上。这些基中,使用抗蚀物时,透光性优越的为:1~6碳的直链或分支烷基、羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。耐干腐蚀性强的为甲基、乙基。这些基中,使用抗蚀物时,对于基板的附着性优越的为:羟基、羟甲基、羟乙基。这些基中同样的可有二个以上。
此聚合体为下述通式(19)
其中,R17~19、W4与通式(12)相同。
从所表示的单体中选择一种以上进行重合。使通式(19)中的单体重合或共同重合。也可与通式(19)中的单体以外的单体共同重合。
上述通式(19)的单体的示例为下述通式(II-1)~(II-18)所表示的单体
(II-1) (II-2) (II-3)
(II-4) (II-5) (II-6)
(II-7) (II-8) (II-9)
其中,R18与上述通式(19)相同。
(II-10) (II-11) (II-12)
(II-13) (II-14) (II-15)
(II-16) (II-17) (II-18)
其中,R18与上述通式(19)相同。
在使用抗蚀物时,耐干腐蚀性优越的为上述通式(II-1)~(II-9)的单体。
上述单体的一例可用下面的通式制造出来
(方案2)
2-对苯金刚烷基、1-金刚烷甲酮及导通衍生物的原料酮可从市面购买或用已知的制法合成。
酸性条件下,从酮与羟基羧可得出已众所周知。反应溶解液以甲苯、环乙烷、乙烷等低溶解性溶解液为宜,为提高收效应除水。
乙醇的脂化反应,可用在通常的脂化条件下进行。作为反应剂可使用(甲)丙烯基酸卤化物、(甲)丙烯基酸无水物、(甲)丙烯基酸脂及(甲)丙烯基酸等,也可用酸、盐基、路易氏酸等。
上述反应的生成物中含有多种构造异性体、几何异性体、光学异性体。在本发明中,即使含有异性体的混合物或中间体也可使用。如有必要,可使用通常的蒸馏、再结晶或光柱谱等方法进行精制。
本发明中的衍生物的第一项为下述通式(7)
其中,R6、R7可相同或不同,表示氢、1~6碳的直链或分支烷基、4~16碳的环烃、含4~16碳的环烃的1~6碳的直链或分支烷基,
R6和R7相结合可以形成4~16碳的环烃,所述烷基,环烃可含1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。
从所表示的单位中选择1种以上构成单位的聚合体,聚合体中衍生物至少含有一种。
上述通式(7)中R6、R7的示例可以是:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基、环戊基、环己基、环庚基、2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基、环己叉等,同样的可含有二个以上。
另外,R6与R7结合在一起的碳原子即形成的桥连环烃为金刚烷基与原菠烷基等。
以上构造可含有1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。这些基中同样的可含有二个以上。
上述通式(7)中的单位的最佳示例为:R6为氢原子、甲基、乙基,R7为环戊基、环己基、环庚基,R6、R7的结合在一起的碳原子共同形成了5~8碳的环烃,如与通式(1)中的单位相同更好。
本发明的衍生物的第二项为下述通式(13)
其中,W5表示直接结合1~6碳的亚甲链,
W6表示直接结合1~3碳的亚甲链,
W7表示1~3碳的亚甲链,
R20指氢原子和甲基,
R21、R22可相同或不同,表示氢原子和1~6碳的直链或分支烷基,4~16碳的环烃和含4~16碳的环烃的1~6碳的直链或分支烷基,
R21和R22相结合可以形成4~16碳的环烃,
所述1~6碳的亚甲链可含1~3碳的烷基,其中可含有一个以上的醚键,所述1~3碳的亚甲链可含有羰基,所述烷基,环烃可含有1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基和1~6碳的乙醇和被酯化的羧基。
从所表示的单位中选择一种以上构成单位聚合体,聚合体中衍生物至少含有一种。
上述通式(13)中的作为W5的示例直接结合(指与W1相邻的氧及碳原子直接结合)CH2、CH2CH2、CH2CH2CH2、CH(CH3)CH2、CH2O、CH2CH2O、CH2CH(CH3)O、CH(CH3)CH2O、CH2CH2OCH2CH2O、CH2CH(CH3)OCH2CH(CH3)O、CH(CH3)CH2OCH(CH3)CH2O等。W5可含有1~3碳的烷基的取代基和一个以上的醚键。从聚合体的保持安定性的角度出发,W5直接结合以CH2、CH2CH2O、CH2CH(CH3)O为好。
作为W6的示例直接结合(指与W5相邻的氧及碳原子直接结合)CH2、C(O)、CH2CH2、CH2C(O)、CH2CH2CH2、CH2C(O)CH2等。从聚合体保持安定的角度出发、直接结合(指与W相邻的氧及碳原子直接结合)CH2、C(O)、CH2C(O)为宜。
作为W7的示例,如:CH2、C(O)、CH2CH2、CH2C(O)、CH2CH2CH2、CH2C(O)CH2等,从聚合体保持安定的角度出发,以CH2、C(O)、CH2C(O)为宜。
上述通式(13)中R21、R22的示例为:氢原子、甲基、乙基、丙基、异丙基、丁基、tert-丁基、环戊基、环己基、环庚基、2-原菠烷基、1-金刚烷基、1-金刚烷甲基、1-金刚烷乙基、2-金刚烷基、2-金刚烷甲基、2-金刚烷乙基等。这些基中同样的可含有二个以上。
R6与R7结合在一起的碳原子即形成的桥连环烃为金刚烷基、原菠烷基和环己基等。
以上构造可含有1~6碳的直链或分支烷基,甚至含有羟基、羧基、2~6碳的酰基、1~6碳的烷氢基和1~6碳的乙醇和被酯化的羧基。这些基中同样的可含有二个以上。
上述通式(13)所表示的单位的示例可以是:R21为氢原子、甲基、乙基,R22为环戊基、环己基、环庚基,R21、R22结合在一起形成5~12碳的环烃,如与通式(11)或(12)中所表示的单位相同更好。
根据本发明,至今为止的位置型抗蚀剂、负型抗蚀剂、防止反射膜材料、绝缘膜材料等已知的耐干腐蚀型向上基、含有酸解性的溶解性基的丙烯酸衍生物、甲基丙烯酸衍生物、丙烯酸、甲基丙烯酸、马来酸、富马酸等具有丙烯基可溶性,与己烯性二重结合的羧酸、丙烯树脂等制造时使用的众所周知的单体共同重合所得到的单位,可与从上述单位中选择一种以上进行适当组合。
上述的丙烯酸衍生物可以是:丙烯酸tert-甲基、丙烯酸四氢呋喃、丙烯酸四氢化吡喃、丙烯酸与2-羟基-3-松莰酮与脂等的羧基的氢氧基,用酸解性取代基进行保护得到的丙烯酸脂、或丙烯酸金刚烷基、丙烯酸环己基、丙烯酸萘基、丙烯酸苄基、丙烯酸3-氧(代)环己基、丙烯酸萜品醇等的脂,丙烯酸与3-溴丙酮等脂,羧的氢氧基用酸不解性取代基进行保护得到的丙烯酸脂。也可把作为甲基丙烯酸衍生物的丙烯酸衍生物对应甲基丙烯酸衍生物列举出来。
另外,具有乙烯性二重结合的羧酸可以是:马来酸、富马酸以及取原菠烷中一部分的烷基、烷氧化基、氢氧基、羟烷基、羧烷基、烷氧化羧基、环己基乙烯醚、羟乙基乙烯醚等乙烯醚衍生物的单体,苯乙烯、对羟苯乙烯、对tert-丁氧苯乙烯的苯乙烯衍生物的单体及无水马来酸等。
丙烯树脂制造所用的是众所周知的单体,如:含有丙烯酸、甲基丙烯酸等的羧酸的氢原子的、甲基、乙基、n-己基、辛基、十二烷基、2-羟乙基、2-羟丙基、环戊基、环己基、2-羟乙基、原菠烷基、三环癸基、
聚合体,化学增幅型抗蚀组成物及形成方法专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0