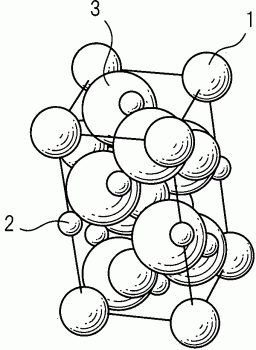
IPC分类号 : B01J23/08,B01J35/00,H01M4/00
专利摘要
本发明提供对通过水分解制造氢具有更高活性的光催化剂和包含所述光催化剂的光电极。本发明的水分解用光催化剂包含Ga的硒化物、Ag-Ga的硒化物或其两者。
权利要求
1.一种水分解用光催化剂,包含Ga的硒化物、Ag-Ga的硒化物或其两者。
2.根据权利要求1所述的水分解用光催化剂,包含Ga的硒化物和Ag-Ga的硒化物两者。
3.根据权利要求1或2所述的水分解用光催化剂,其中所述Ga的硒化物选自由GaSe、Ga2Se3及其组合组成的群。
4.根据权利要求3所述的水分解用光催化剂,其中所述Ga的硒化物是GaSe。
5.根据权利要求1至4中任一项所述的水分解用光催化剂,其中所述Ag-Ga的硒化物选自由AgGaSe2、AgGa5Se8及其组合组成的群。
6.根据权利要求5所述的水分解用光催化剂,其中所述Ag-Ga的硒化物是AgGaSe2。
7.根据权利要求1至6中任一项所述的水分解用光催化剂,其中所述光催化剂进一步包含负载于其上的Rh和Pt中的至少一种。
8.一种水分解用光电极,包含基板、形成于所述基板上的导电层、以及形成于所述导电层上且由根据权利要求1至7中任一项所述的水分解用光催化剂组成的光催化剂层。
说明书
技术领域
本发明涉及水分解用光催化剂,更具体地,使用能量如太阳光来制造氢的水分解用光催化剂,以及包含所述光催化剂的水分解用光电极。
背景技术
氢作为清洁燃料已引起了注意,因为它的燃烧不产生二氧化碳。然而,氢的工业制造依赖于化石燃料,因此在氢的制造过程中放出二氧化碳。因此,即使使用氢作为燃料,也不能解决化石燃料的耗竭和由二氧化碳造成的全球变暖。因此,已把大量注意力集中到能够使用自然能如太阳光来分解水而制造氢的光催化剂。
日本未审查专利公开(Kohyo)2010-519057号描述了至少一种纳米粒子作为多种化学反应如氧化还原反应和水分解的光催化剂的用途,其中所述至少一种纳米粒子包含至少一个金属/金属合金区域和在可见(400-700nm)到近红外(NIR)范围(0.7-3μm)具有吸收开始的至少一个半导体区域,其中所述至少一个半导体区域是III-VI族的且选自InSe、InTe、InS、GaSe、InGaSe、InSeS、以及它们的合金。
日本未审查专利公开(Kokai)2010-046604号描述了一种光催化剂,其使用化合物A,所述化合物A包含具有dn(0<n<10)型电子构型的金属离子、氧离子(O2-)以及选自如下的至少一种元素B的离子:H、Li、Na、K、Rb、Cs、Mg、Ca、Sr、稀土元素、Ti、Zr、Hf、V、Nb、Ta、Mo、W、Cu、Ag、Au、Zn、Cd、Al、Ga、In、C、Si、Ge、Sn、N、P、Sb、S、Se、Te、F、Cl、Br和I(条件是当元素B是金属元素时,所述元素B的离子具有除dn(0<n<10)型电子构型以外的电子构型)。日本未审查专利公开(Kokai)2010-046604号还描述了可通过在照射光的同时使这种光催化剂与含氢化合物接触来制造氢。
发明内容
如上所述,日本未审查专利公开(Kohyo)2010-519057号描述了包含各种金属/金属合金与半导体的组合的纳米粒子作为多种化学反应的光催化剂的用途。然而,日本未审查专利公开(Kohyo)2010-519057号未具体公开纳米粒子在用于水分解反应中时的水分解活性。类似地,日本未审查专利公开(Kokai)2010-046604号未具体公开作为光催化剂的上述化合物A在用于水分解反应中时的水分解活性。
另一方面,为了使光催化剂在水分解反应中有效地起作用,一般优选的是,光催化剂的导带最小值(CBM)和价带最大值(VBM)处于将水的还原电位与氧化电位夹在其间的位置。
例如,Cu基黄铜矿材料如Cu(In,Ga)(Se,S)2一般是显示p型传导性的半导体材料并且典型地以多晶状态用于薄膜太阳能电池等中,并且已知这种材料的有利之处在于例如对应于从VBM到CBM的能量差的带隙可以通过改变其组成来控制。然而,Cu(In,Ga)(Se,S)2材料的VBM与水的氧化电位相比相当低,因此即使将这种材料用于水分解用光催化剂、光电极等中,也不能获得充分的水分解活性。
因此,本发明的目的是提供对通过水分解制造氢具有更高活性的光催化剂和包含所述光催化剂的光电极。
用于实现该目的的本发明如下。
(1)一种水分解用光催化剂,包含Ga的硒化物、Ag-Ga的硒化物或其两者。
(2)如项(1)所述的水分解用光催化剂,包含Ga的硒化物和Ag-Ga的硒化物两者。
(3)如项(1)或(2)所述的水分解用光催化剂,其中所述Ga的硒化物选自由GaSe、Ga2Se3及其组合组成的群。
(4)如项(3)所述的水分解用光催化剂,其中所述Ga的硒化物是GaSe。
(5)如项(1)至(4)中任一项所述的水分解用光催化剂,其中所述Ag-Ga的硒化物选自由AgGaSe2、AgGa5Se8及其组合组成的群。
(6)如项(5)中所述的水分解用光催化剂,其中所述Ag-Ga的硒化物是AgGaSe2。
(7)如项(1)至(6)中任一项所述的水分解用光催化剂,其中所述光催化剂进一步包含负载于其上的Rh和Pt中的至少一种。
(8)一种水分解用光电极,包含基板、形成于所述基板上的导电层、以及形成于所述导电层上且由项(1)至(7)中任一项所述的水分解用光催化剂组成的光催化剂层。
附图说明
图1是示出对应于Cu(In,Ga)(Se,S)2材料的CuGaS2和CuGa5S8的状态密度(DOS)的示意图。
图2是由半导体材料实现的水分解的概念图。
图3是示出作为Ag-Ga的硒化物之一的AgGaSe2的晶体结构的示意图。
图4示出了实施例1~8的样品的XRD图。
图5示出了实施例1、3以及8的样品的UV-Vis DRS的测量结果。
图6示出了通过UV-Vis DRS测量的实施例1~8的样品的吸收端波长。
图7示出了分别具有0、0.17、0.48以及0.75的Ag/Ga比率的样品的空气中的光电子光谱的测量结果。
图8示出了实施例9中的样品(a)~(i)的带隙的位置。
图9是光电化学测量中所用的装置的示意图。
图10示出了三个水分解用光电极,即,包含Ag/Ga比率为0.15的光催化剂层的水分解用光电极以及进一步包含负载于其上的Rh的水分解用光电极和进一步包含负载于其上的Pt的水分解用光电极的光电化学测量的结果。
图11示出了其上负载有Rh的水分解用光电极(Ag/Ga比率=0、0.06、0.15以及0.55)的光电化学测量的结果。
图12示出了Ag/Ga比率为0.15的负载有Rh的光电极的电流-时间曲线与氢生成量之间的关系。
具体实施方式
本发明的水分解用光催化剂包含Ga的硒化物、Ag-Ga的硒化物或其两者。
如上所述,已知Cu基黄铜矿材料如Cu(In,Ga)(Se,S)2一般显示p型传导性,并且其带隙等可以通过改变其组成来控制。
图1是示出对应于Cu(In,Ga)(Se,S)2材料的CuGaS2和CuGa5S8的状态密度(DOS)的示意图。参考图1,在CuGaS2与CuGa5S8两种材料中,价带最大值(VBM)由Cu的3d轨道构成,并且导带最小值(CBM)的位置跨过对应于带隙的禁带。如图1中所示,CuGaS2和CuGa5S8的VBM的电位基于标准氢电极(NHE)分别是0.7VNHE和0.9VNHE。
另一方面,为了使上述半导体材料在水分解中有效地充当光催化剂,如上所述,通常优选的是,半导体材料的CBM和VBM处于将水的还原电位与氧化电位夹在其间的位置。更具体地,如图2的概念图中所示,使用半导体材料的水分解的基本概念是通过照射光将半导体材料的价带(VB)中存在的电子激发到导带(CB),并且产生的电子(e-)和空穴(h+)通过氧化还原反应分解水。顺便提及,水的氧化还原反应由以下化学反应式表示:
还原反应:H++e-→1/2H2 E0=0V
氧化反应:H2O→l/2O2+2H++2e- E0=1.23V
这种氧化还原反应是其中电子移动的反应,因此要求其是显示负吉布斯(Gibbs)能量变化以引起反应的反应,即其中电子转移到更低的氧化还原水平的反应。因此,为了满足这种条件,优选的是,半导体材料的CBM和VBM处于将水的还原电位与氧化电位夹在其间的位置,即,基于标准氢电极(NHE),VBM>1.23VNHE且CBM<0VNHE。当满足这种要求时,理想地,可以使得在无外部施加电压的情况下仅通过半导体材料的光催化作用而进行水分解反应。或者,即使不完全满足这种要求,也可以通过提供尽可能与之相近的条件使用半导体材料来减少水分解反应中所需要的外部施加电压。
对应于Cu(In,Ga)(Se,S)2材料的CuGaS2和CuGa5S8各自的CBM的电位低于0VNHE,因此满足CBM<0VNHE的要求。然而,如图1中所示,CuGaS2和CuGa5S8的VBM的电位分别是0.7和0.9VNHE,这相当低于1.23VNHE,因此不满足VBM>1.23VNHE的要求。
本发明人已注意并研究了其中用Ag置换Cu的Cu基黄铜矿材料如Cu(In,Ga)(Se,S)2,并且发现包含Ga的硒化物、Ag-Ga的硒化物或其两者的材料与类似的Cu基黄铜矿材料相比具有更高的基于NHE的VBM。此外,本发明人发现,当将这种材料用于水分解用光催化剂中时,在各种组合物中获得了高水分解活性。
根据本发明,Ga的硒化物包括但不特别限于例如选自由GaSe、Ga2Se3以及其组合组成的群的化合物,并且优选为GaSe。
根据本发明,Ag-Ga的硒化物包括但不特别限于例如选自由AgGaSe2、AgGa5Se8以及其组合组成的群的化合物,并且优选为AgGaSe2。
图3是示出作为Ag-Ga的硒化物之一的AgGaSe2的晶体结构的示意图。在图3中,标号“1”表示Ag,标号“2”表示Ga,并且标号“3”表示Se。该AgGaSe2具有黄铜矿型晶体结构和约1.6~1.8eV的带隙(O.Madelung,U.Rossler,M.Schulz,The Landolt-Bornstein Database,硒化银镓(AgGaSe2)能隙(silver gallium selenide(AgGaSe2)energy gaps),Springer Materials),并且已经报导了p型半导体与n型半导体两者(Nigge,KM.等人,太阳能材料太阳能电池(Sol.Energy Mater.Sol.Cells)43(1996)335)。
在作为Cu基黄铜矿材料的CuGaSe2中,一般已知诸如CuGa3Se5和CuGa5Se8的组合物的缺陷相可以通过减少其中所含的Cu元素而形成。因此,认为在具有相同黄铜矿型晶体结构的AgGaSe2中发生类似的现象,即,认为在制备AgGaSe2时,例如通过适当地选择Ag/Ga比率等可以将诸如AgGa5Se8的化合物形成为AgGaSe2的缺陷相。
在本发明的实施方式中,本发明的水分解用光催化剂可以为含有上述Ga的硒化物和Ag-Ga的硒化物中的任一种的单晶的形式,或可以为含有上述Ga的硒化物和Ag-Ga的硒化物中的任两种以上的多晶的形式。顺便提及,在使用多晶形式的本发明的水分解用光催化剂的情况下,多晶中所含的各单晶的比例无特别限制,并且可根据使用本发明的水分解用光催化剂的条件等而确定。
本发明的水分解用光催化剂可以以薄膜与粉末两种形式使用,并且其形式可以根据使用本发明的水分解用光催化剂的实施方式等而适当地选择。例如,在使用其中将本发明的水分解用光催化剂分散在水中的悬浮体系的水分解的情况下,本发明的水分解用光催化剂可以以粉末的形式使用。另一方面,在电极系统中使用本发明的水分解用光催化剂的水分解的情况下,本发明的水分解用光催化剂可以以薄膜的形式使用。
本发明的水分解用光催化剂可以通过本领域技术人员已知的任何方法制造。例如,在以薄膜形式使用本发明的水分解用光催化剂作为光电极的情况下,光电极可以例如如下制造。
首先,例如在室中布置透明基板如玻璃以作为光电极的基板。然后,在减压下,在基板上沉积导电层以作为集电极。顺便提及,可以根据构成导电层的金属的类型通过适当手段合适地进行沉积,特别地,当使用高熔点材料如Mo等作为导电层时,优选通过溅射进行沉积。另外,在这种情况下,为了提高导电层与基板之间的粘合性,可以在沉积导电层之前,在基板上任选地沉积其他金属如钛(Ti)等以作为粘合层。
然后,使用例如真空沉积法等在导电层上沉积由包含Ga的硒化物、Ag-Ga的硒化物或其两者的本发明的水分解用光催化剂组成的光催化剂层。具体来说,可以通过在加热下从单独的舟皿或坩埚中蒸发构成Ga的硒化物或Ag-Ga的硒化物的银(Ag)、镓(Ga)以及硒(Se)的各金属材料并且使其沉积在导电层上而在导电层上形成包含Ga的硒化物、Ag-Ga的硒化物或其两者的光催化剂层。顺便提及,在导电层上沉积仅包含Ga的硒化物的光催化剂层的情况下,可仅使用Ga和Se的各金属材料进行相同操作。沉积各金属元素的顺序无特别限制,例如可同时沉积Ag、Ga以及Se,或可在Ag和Ga的沉积之后沉积Se。然而,不优选在Ag和Ga的沉积之前沉积Se,因为Se与其他两种金属元素相比具有更低的沸点并且可能在Ag或Ga的沉积期间在高温下蒸发。
或者,沉积由本发明的水分解用光催化剂组成的光催化剂层的另一种方法可包括例如在含硒气体气氛中、特别是在硒化氢(H2Se)气体中在预定温度下对基板进行热处理,其中基板包含导电层和通过溅射或真空沉积方法沉积在其上的Ag和/或Ga。这种方法也使得可以在导电层上形成包含Ga的硒化物、Ag-Ga的硒化物或其两者的光催化剂层。
例如,在通过上述真空沉积方法将Ag、Ga以及Se的各金属元素依次分别沉积的情况下,可以通过使用任何合适手段以适当的厚度沉积各金属元素来控制最终获得的光催化剂层中Ga的硒化物和Ag-Ga的硒化物的组成比。例如,如果完全不沉积Ag,则当然可以选择性地产生Ga的硒化物如GaSe和Ga2Se3,或者如果以使得Ag的量小于Ga的量的方式沉积Ag层,则除了上述Ga的硒化物以外,与AgGaSe2相比,可以选择性地沉积AgGa5Se8等作为Ag-Ga的硒化物。另一方面,当沉积的Ag的量增加时,可以防止产生Ga的硒化物或AgGa5Se8,并且可以选择性地产生主要含有AgGaSe2的Ag-Ga的硒化物。
如上所述,本发明的水分解用光催化剂包含Ga的硒化物、Ag-Ga的硒化物或其两者。然而,本发明的水分解用光催化剂可进一步包含其他成分,尤其是促进剂。例如,对通过水分解制造氢来说,本发明的水分解用光催化剂单独不一定能获得充分的反应速率。在这种情况下,可以通过在本发明的水分解用光催化剂上负载例如贵金属,尤其是Rh和Pt中的至少一种作为促进剂来促进通过水分解制造氢。
可通过本领域技术人员已知的任何方法来进行金属如Rh和Pt的负载。例如,可以通过如下进行金属的负载:提供含有金属阳离子的化合物作为金属源,将本发明的水分解用光催化剂浸渍在以预定浓度含有该化合物的电解液中,并且使用氙(Xe)灯等利用光对电解液进行照射。因为这使得与氢离子的还原反应相比,可以通过光催化剂的催化作用而优先进行光催化剂表面上的金属离子的还原反应,所以可以在光催化剂的表面上将金属离子沉积为金属。金属的负载量无特别限制,并且可根据期望的光催化性能而确定。
使用本发明的水分解用光催化剂的水分解反应可以通过本领域技术人员已知的任何方法进行。例如,可通过如下分解水而产生氢:使用粉末形式的本发明的水分解用光催化剂,将其分散于水中并且利用来自作为光源的Xe灯的光照射分散液,同时根据需要进行搅拌。或者,可通过如下分解水而产生氢:将薄膜形式的本发明的水分解用光催化剂与导电膜等组合以构成光电极,并且将光电极与作为对电极的铂电极等一起布置于水中,并且利用来自也用作光源的Xe灯等的光照射光电极。
下面基于实施例更详细地描述本发明,但本发明不限于这些实施例。
实施例
在以下实施例中,制造包含由本发明的水分解用光催化剂组成的光催化剂层的水分解用光电极,并且对所制造的光电极检验在0~1.2的范围内改变光催化剂层中所含的Ag与Ga之间的原子比(Ag/Ga比率)的影响和效果。
[实施例1]
[光电极的制造]
首先,将面积为5×10mm2的钠钙玻璃(SLG)在乙醇中进行超声清洗,并且用作基板。然后,将基板插入到RF磁控溅射装置的室中,并且将室内部抽真空到约10-4Pa的压力。然后,在200℃的基板温度、100W的溅射功率以及8×10-2Pa的Ar分压的条件下,使用Ar等离子体在SLG基板上溅射Ti并持续5分钟以沉积Ti层作为粘合层,并且随后在Ti层上溅射Mo并持续20分钟以沉积Mo层作为集电极。
其次,在分子束外延(MBE)装置中在300℃下加热获得的Mo/Ti/SLG基板的同时,使用石英振荡器膜厚度计以0.08~0.11nm/s的沉积速率在Mo层上真空沉积Ga以沉积厚度为700nm的Ga薄膜。然后,将获得的Ga薄膜暴露于Se蒸气并同时在MBE装置中对其进行加热以使Ga薄膜硒化,从而最终获得包含无Ag(即Ag/Ga比率=0)光催化剂层的水分解用光电极。顺便提及,在硒化期间,MBE装置中的压力<5×10-6Pa,基板温度是300~500℃,硒化时间是60~180分钟,并且Se供应速率是0.6~1.0nm/s。
[实施例2~8]
在实施例2~8中,以与实施例1中相同的方式获得包含Ag/Ga比率分别为0.06、0.17、0.24、0.55、0.60、0.77和1.20的光催化剂层的水分解用光电极,不同之处在于,在Mo/Ti/SLG基板上真空沉积Ga之前以0.4~0.5nm/s的沉积速率在Mo层上真空沉积Ag、并且将Ag薄膜和Ga薄膜沉积到使Ag/Ga比率(原子比)为0.06~1.20的厚度。
[光催化剂层的分析]
通过X射线衍射(XRD)来测量实施例1~8中获得的各样品。图4示出了实施例1~8的样品的XRD图。
参考图4,在Ag/Ga比率接近1,特别地Ag/Ga比率≥0.6时,主要检测到来自AgGaSe2的衍射峰,并且在Ga过量,特别地Ag/Ga比率<0.3时,主要检测到来自GaSe的衍射峰。通过引用来自文献(H.Ishizaki,K.Yamada,R.Arai,Y.Kuromiya,Y.Masatsugu,N.Yamada and T.Nakada,Mater.Res.Soc.Symp.Proc.865,(2005)143)的AgGa5Se8的晶格常数并且在AgGa5Se8具有与AgIn5Se8相同的结构的假设下进行计算(所用软件:CaRIne v3.1)而获得AgGa5Se8的XRD图。关于Ga2Se3和AgGa5Se8的衍射峰,因为在几乎相同位置检测到Ga2Se3的(130)和(031)面与AgGa5Se8的(112)面的衍射峰,并且在几乎相同位置检测到Ga2Se3的(133)和(331)面与AgGa5Se8的(204)面的衍射峰,所以不能将它们明确地区分。顺便提及,在实施例1~8的各样品中,在2θ=40°附近检测到的大衍射峰可归因于作为集电极的Mo层。
随后,通过UV-Vis DRS(紫外线-可见漫反射光谱法)测量实施例1、3以及8的各样品。图5示出了实施例1、3以及8的样品的UV-Vis DRS的测量结果。
参考图5,在Ag/Ga比率是0的实施例1的样品中,在约590nm和约650nm处观察到光吸收。认为两种吸收端都与Ga的硒化物有关。此外,在Ag/Ga比率分别是0.17和1.2的实施例3和8的样品中,在约700nm处观察到推测是源自AgGaSe2的光吸收。
此外,通过UV-Vis DRS测量实施例1~8的样品的吸收端波长,并且将结果绘制在图6中。图6示出了通过UV-Vis DRS测量的实施例1~8的样品的吸收端波长。在图6中,横轴表示Ag/Ga比率(原子比),并且纵轴表示吸收端波长(nm)。参考图6,在Ag/Ga比率是0和0.06的实施例1和2的样品中,分别在650和660nm的短波长侧检测到吸收端。另一方面,在Ag含量更高的实施例3~8的样品中,在约700~710nm的范围内存在吸收端,因此发现除了接近0的Ag/Ga比率之外,吸收端不随Ag/Ga比率的波动而大大变化。一般已知,样品的带隙可通过测量UV-Vis光谱而由其吸收端波长确定,并且当吸收端波长移动到较短波长侧时,带隙变得更大。因此,由图5和6的结果可以理解,Ag/Ga比率分别为0和0.06的实施例1和2的样品,与Ag/Ga比率更大的实施例3~8的样品相比,带隙更大,并且在实施例3~8的样品之间带隙无大差异。
[实施例9]
在本实施例中,以与实施例1~8相同的方式制造总计9个样品,其中光催化剂层中所含的Ag与Ga之间的原子比(Ag/Ga比率)是(a)0,(b)0.11,(c)0.17,(d)0.19,(e)0.23,(f)0.48,(g)0.59,(h)0.65以及(i)0.75,并且计算各样品的导带最小值(CBM)和价带最大值(VBM)。
首先,通过空气中的光电子光谱测量样品(a)~(i)。图7示出了这些样品中的4个样品的数据。图7示出了具有(a)0,(c)0.17,(f)0.48以及(i)0.75的Ag/Ga比率的样品的空气中的光电子光谱的测量结果。在图7中,横轴表示照射光的能量,并且纵轴表示光电子收率的0.33次幂。如图7中所示,由光电子收率与背景的交点处的能量计算电离电位。
随后,基于由空气中的光电子光谱计算的电离电位和由UV-VisDRS的吸收端波长计算的带隙来计算所有样品(a)~(i)的CBM和VBM的电位。将其结果显示在图8中。图8示出了实施例9中的样品(a)~(i)的带隙的位置。在图8中,横轴表示Ag/Ga比率(原子比),并且纵轴表示基于NHE(标准氢电极)的电位(相对于NHE的V)。顺便提及,图8中的虚线分别表示水的还原电位(0VNHE)和氧化电位(1.23VNHE)。
参考图8,在Ag/Ga比率为0的样品(a)中,发现其CBM和VBM处于将水的还原电位与氧化电位夹在其间的位置,也就是满足VBM>1.23VNHE且CBM<0VNHE的要求。因此,按照CBM和VBM的位置,认为样品(a)具有最优选的带结构和高光电化学性能。另一方面,在样品(b)~(i)中,发现CBM和VBM的电位显示基本恒定的值,尽管它们因Ag/Ga比率的变化而略微波动。虽然样品(b)~(i)都不满足VBM>1.23VNHE的要求,但发现与图1中所示的作为Cu基黄铜矿材料的CuGaS2(VBM=0.7VNHE)和CuGa5S8(VBM=0.9VNHE)相比,所有这些样品都具有更高的基于NHE的VBM。
[实施例10]
[光电化学测量]
在本实施例中,以与实施例1~8相同的方式制造包含Ag/Ga比率为0.15的光催化剂层的水分解用光电极,并且使用图9中所示的装置对其进行光电化学测量。在光电化学测量中,通过铟(In)将导线附着至水分解用光电极的Mo层,并且将不必要的部分用环氧树脂覆盖且防止其与电解液接触。
图9是光电化学测量中所用的装置的示意图。在本装置中,使用本发明的水分解用光电极作为工作电极11,使用Pt线作为对电极12,并且使用Ag/AgCl电极作为参比电极13。另外,根据需要通过磁力搅拌器15等进行搅拌,并且在由恒电位器14(HSV-100,由北斗电工株式会社(Hokuto Denko Corporation)制造)控制电位的同时,测量通过工作电极11的电流。顺便提及,扫描速度是5mV/s,并且根据能斯特方程(Nernst equation)基于可逆氢电极(RHE)对电位进行换算。此外,为了确保充分的导电性,使用0.1M Na2SO4水溶液作为电解液,并且通过添加NaOH水溶液而将电解液的pH调节为9。在测量之前,将Ar气吹到溶液中以除去溶解氧。使用配备有冷光镜和截止滤光片(L-42,由HOYA制造)的300W的Xe灯(λ=420~800nm)作为光源。通过使用百叶窗以3秒的间隔重复光的照射和阻挡来间歇式照射光,并且测量光照射期间的暗电流和电流。
此外,在本实施例中,为了检验光催化剂被金属表面改性的效果,还对进一步包含负载在上述水分解用光电极的光催化剂层上的Rh或Pt的光电极进行光电化学测量。顺便提及,Rh或Pt在光催化剂层上的负载通过光电沉积法来进行。具体来说,使用图9的装置,向100ml0.1MNa2SO4水溶液(pH=9)中添加0.4μmol Na3RhCl6,并且将包含光催化剂层的水分解用光电极浸渍在所得溶液中。然后,将电位保持在相对于Ag/AgCl为-0.4V下,并且通过光照射30~200分钟使Rh离子还原,直至光电流值饱和,从而在光催化剂层上沉积Rh。以与Rh的情况中相同的方式进行在光催化剂上负载Pt,不同之处在于,向100ml0.1M Na2SO4水溶液(pH=9)中添加H2PtCl6并且将保持电位改为相对于Ag/AgCl为-0.7V。
对三种水分解用光电极进行光电化学测量,即,包含Ag/Ga比率为0.15的光催化剂层的水分解用光电极以及进一步包含负载于其上的Rh的水分解用光电极和进一步包含负载于其上的Pt的水分解用光电极。图10示出了结果。在图10中,横轴表示基于RHE(可逆氢电极)的电位(相对于RHE的V),并且纵轴表示电流密度(mA/cm2)。
如上所述,通过以3秒的间隔间歇照射光而进行光电化学测量。参考图10,确认了,在三种水分解用光电极的每一种中,通过打开或关闭光照射而使得电流流动。此外,从图10的结果可见,在其上负载有Rh的水分解用光电极中获得最高电流密度。此外,关于各水分解用光电极,通过恒电位器从低电位侧向高电位侧扫描电位以检测图10中的箭头所示的电流开始流动的电位,并且将检测到的电位定义为光电流开始电位。下表1示出了各水分解用光电极的光电流开始电位(VRHE)和0.1VRHE下的电流密度(mA/cm2)。
表1:包含Ag/Ga比率为0.15的光催化剂层的光电极的光电化学测量
从图10和表1的结果发现,所有光电极都显示水分解活性,无论是否被金属表面改性。尤其是,发现负载有Rh的光电极在光电流开始电位与电流密度两方面都显示高值,因此显示最高水分解活性。
[关于负载有Rh的光电极的Ag/Ga比率的影响]
其次,对在上述光电化学测量中显示最高水分解活性的负载有Rh的光电极检验改变Ag/Ga比率的影响。具体来说,通过以与上述说明相同的方式在Ag/Ga比率分别是0、0.06、0.15以及0.55的光催化剂层上负载Rh来制造水分解用光电极,并且对这些水分解用光电极的每一个进行光电化学测量。图11示出了结果。另外,下表2示出了从图11获得的水分解用光电极的光电流开始电位(VRHE)的值(在图11中由箭头所示)。
表2:关于负载有Rh的光电极的Ag/Ga比率的影响
参考图11和表2的结果,关于电流密度,在Ag/Ga比率=0的负载有Rh的电极中获得最高值。然而,关于光电流开始电位,Ag/Ga比率=0.15的负载有Rh的电极显示最高值。另一方面,如关于图8所述,图8的结果表明,包含Ag/Ga比率=0的光催化剂层的光电极对于水分解来说具有最优选的带结构,因此具有高光电化学性能。因此,图11的结果与图8的结果之间不一定完全一致。
不希望受任何特定的理论束缚,在一些测量样品中,例如,在Ag/Ga比率=0的测量样品中,在高电位侧观察到光阳极响应,因此认为样品的一部分转变为n型。此外,认为这种样品到n型的部分转变在从图8中所示的CBM和VBM的位置预期的结果与由光电化学测量获得的结果之间造成差异。
[氢生成量与光电流值之间的关系]
对在使用Ag/Ga比率=0.15的负载有Rh的光电极的光电化学测量中产生的气体进行分析,并且图12示出结果。
图12示出了Ag/Ga比率为0.15的负载有Rh的光电极的电流-时间曲线与氢生成量之间的关系。在图12中,横轴表示时间(分钟),左侧纵轴表示在相对于Ag/AgCl为-0.7V的电极下通过对电极的电流值(mA),并且右侧纵轴表示由气相色谱法的峰面积计算的氢生成量(μmol/小时)(每3分钟进行测量)。在图12中,显示左侧纵轴和右侧纵轴上的值在理论上彼此对应。参考图12,发现在光电化学测量中观察到的电流值与生成的氢的量几乎一致。该结果显示,在包含本发明的水分解用光催化剂的光电极中,将几乎100%的光电流用于水的还原。
工业实用性
本发明的水分解用光催化剂与类似的Cu基黄铜矿材料如Cu(In,Ga)(Se,S)2相比具有更高的基于NHE(标准氢电极)的价带最大值(VBM)。因此,通过在水分解用光电极中使用这种光催化剂可以获得更高的水分解活性。
包含镓的硒化物的水分解用光催化剂和包含所述光催化剂的水分解用光电极专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0