IPC分类号 : C07C69/757,C07J1/00,C12P33/00,C12P15/00,A61P25/28,C12R1/66
专利摘要
本发明提供了具有抗阿尔茨海默病作用的新杂萜类化合物及其分离制备方法,该化合物来源于土壤的土曲霉次生代谢产物,本发明通过对土壤来源AspergillusterreusQCX1‑1固体发酵和对其发酵产物的工业酒精(95%乙醇)提取物进行分离纯化,得到3个新化合物。运用多种波谱分析手段和其他方法,确定其结构为杂萜类化合物,通过对这3个新化合物的BACE1抑制活性评价,发现其中2个化合物能够在体内及体外对BACE1产生极强的抑制活性,可以作为治疗抗阿尔茨海默病药物开发的先导化合物。
权利要求
1.具有以下式(1)所示结构的从土壤来源真菌土曲霉中分离纯化得到的杂萜类化合物1-3,
化合物1:土壤土曲霉菌素A(Asperterpenes A)
化合物2:土壤土曲霉菌素B(Asperterpenes B)
化合物3:土壤土曲霉菌素C(Asperterpenes C)
式(1)。
2.权利要求1所述的杂萜类化合物的制备方法,包括以下步骤:
S1.种子培养基的制备:
将分离于长江滩涂的土曲霉Aspergillus terreusQCX1-1菌株接入种子培养基,利用摇床培养并得到种子培养液;上述摇床培养的条件为:摇床转速100~120rpm,培养时间为3~5天,培养温度25~28℃;所述种子培养基的组分为:麦芽膏3g,葡萄糖10g,蛋白胨5g,酵母膏3g及水1L;
S2.接种:
利用固体发酵的方式进行菌种培养,大米固体发酵培养基加入培养瓶中,接种S1中得到的种子培养液,静置培养;所述大米固体发酵培养基均为将大米200g及水200mL加入1L的三角锥形瓶中;所述静置培养温度为25~28℃,培养时间为25~30天;
S3.利用工业酒精提取S2中发酵得到的菌丝体及培养基,减压浓缩回收工业酒精,得到浸膏;
S4.将S3中所得的浸膏经层析分离,得到式(1)中所示化合物1-3;所述层析分离方法包括凝胶柱层析,高效液相色谱及硅胶柱层析。.
3.权利要求1中所述的化合物1和2在制备抗阿尔茨海默病的药物中的应用。
4.根据权利要求3所述的应用,其特征在于,所述的化合物为BACE1抑制剂(β-site amyloid precursor protein cleaving enzyme 1),其中化合物1在3xTg小鼠中表现出较好的抗阿尔茨海默作用,其活性与阳性药LY2811376(礼来公司)基本一致。
说明书
技术领域
本发明属于医药技术领域,涉及抗阿尔茨海默病化合物,具体涉及土壤土曲霉次生代谢产物中的抗阿尔茨海默病化合物及其分离制备方法和用途,主要涉及分离纯化的过程,结构确认,BACE1抑制活性及抗阿尔茨海默病活性考察等。
背景技术
阿尔茨海默病(Alzheimer disease,AD)是一种常见的中枢神经系统变性病,病程呈现慢性进行性,是老年期痴呆最多见的一种疾病类型,据不完全统计,全球该疾病的患病人数高达4860万,其中我国患者数为684万。该疾病的主要表现为认知功能障碍、人格改变、渐进性记忆障碍和语言障碍等,严重影响患者的工作与生活功能。AD的发病机制与病因尚未完全阐明,β淀粉样蛋白沉积形成的细胞外老年斑、tau蛋白过度磷酸化形成的神经细胞内神经原纤维缠结等是该疾病最主要的特征性病理改变。BACE1(β-site amyloid precursor protein cleaving enzyme 1)是AD病发病过程中关键蛋白,能够促进β淀粉样蛋白的沉积,从而加剧疾病的发展,因此,寻找有效的BACE1抑制剂能够对AD病的治疗起到极大的促进作用。
天然产物是药物最常见的来源,据统计,从上世纪八十年代年至今,每年30-40%的上市药物直接或间接来源于天然产物,其中2010年,天然产物相关来源的药物比例高达50%。真菌次生代谢产物的种类极为丰富,随着近年对其研究的不断增多,越来越多化学结构新颖,且活性较强的化合物被发现,为新药的研发奠定了一定的基础。因此,从真菌中分离具有抗阿尔茨海默作用的新的天然产物具有极为重要的意义。
发明内容
本发明的目的是提供具有抗阿尔茨海默作用活性的新的杂萜类化合物及其来源、分离纯化方法和其应用。
本发明提供的具有抗阿尔茨海默作用活性的新的杂萜类化合物为具有以下式(1)所示结构1-3:
化合物1:土壤土曲霉菌素A(Asperterpenes A)
化合物2:土壤土曲霉菌素B(Asperterpenes B)
化合物3:土壤土曲霉菌素C(Asperterpenes C)
式(1)。
本发明提供的具有抗阿尔茨海默作用活性的新的杂萜类化合物的制备方法,包括以下步骤:
S1.种子培养基的制备:
将分离于长江滩涂的土曲霉Aspergillus terreusQCX1-1菌株接入种子培养基,利用摇床培养并得到种子培养液;上述摇床培养的条件为:摇床转速100~120rpm,培养时间为3~5天,培养温度25~28℃;所述种子培养基的组分为:麦芽膏3g,葡萄糖10g,蛋白胨5g,酵母膏3g及水1L;
S2.接种:
利用固体发酵的方式进行菌种培养,大米固体发酵培养基加入培养瓶中,接种S1中得到的种子培养液,静置培养;所述大米固体发酵培养基均为将大米200g及水200mL加入1L的三角锥形瓶中;所述静置培养温度为25~28℃,培养时间为25~30天;
S3.利用工业酒精提取S2中发酵得到的菌丝体及培养基,减压浓缩回收工业酒精,得到浸膏;
S4.将S3中所得的浸膏经层析分离,得到式(1)中所示化合物1-3;所述 层析分离方法包括凝胶柱层析,高效液相色谱及硅胶柱层析。.
本发明提供的新的杂萜类化合物1和2能用于制备抗阿尔茨海默病的药物,所述的化合物1和2为BACE1抑制剂(β-site amyloid precursor protein cleaving enzyme 1),其中化合物1在3xTg小鼠中表现出较好的抗阿尔茨海默作用,其活性与阳性药LY2811376(礼来公司)基本一致。
本发明人通过对土壤来源Aspergillus terreus QCX1-1固体发酵和对其发酵产物的工业酒精(95%乙醇)提取物进行分离纯化,得到3个新化合物。运用多种波谱分析手段和其他方法,确定其结构为杂萜类化合物,具体结构如式(1)所示。通过对化合物1-3的BACE1抑制活性评价,发现化合物1及2能够在体内及体外对BACE1产生极强的抑制活性,可以作为治疗抗阿尔茨海默病药物开发的先导化合物。
附图说明
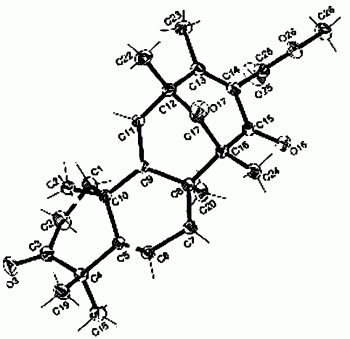
图1:化合物1单晶结构,用于确定该化合物绝对构型。
图2:化合物1与2生源途径,用于确定化合物2绝对构型。
图3:化合物3单晶结构,用于确定该化合物绝对构型。
图4:化合物1(A)和2(B)与BACE1蛋白虚拟对接图,该图提示化合物1和2与BACE1均存在一定的结合。
图5:三个浓度35,70,135nM的化合物1加入N2a-APP细胞中,分别检测其对BACE1活性及Aβ42产量的影响:A)APP-β,APP与DM1A的Western blot分析;B)各组APP-β/APP分析值;C)BACE1活性;D)Aβ42产量,与对照组相比较;***p<0.001,**p<0.01,*p<0.05。由于APP-β/APP直接影响Aβ42的产量,而后者与AD病的发病密切相关,因此对于APP-β/APP的检测能够在细胞层面反应化合物对APP-β及Aβ42的影响,该图显示,化合物1在N2a-APP细胞系中对BACE1具有较好的抑制活性,亦能够降低APP-β及Aβ42的产率。
Figure 5.Compound 1inhibited BACE1activity and decreased Aβ42production.35,70,135nM concentrations of 1added into the medium of N2a-APP cell lines.A)Western blot analysis of protein levels of APP-β,APP and DM1A.B)Quantitative analysis of the ratio of APP-β/APP in the reference groups.C)BACE1activity is determined by beta-Secretase Activity Assay Kit.D)Aβ42levels were quantified through ELISA.Values were shown as mean±SD.***p<0.001, **p<0.01,*p<0.05versus the vehicle group.
图6:利用水迷宫检测化合物1对3xTg AD病小鼠学习与记忆能力的修复与改善作用, 1(2μg/μL×5μL,0.2μg/μL×5μL),LY2811376(2μg/μL×5μL)及空白溶剂注入小鼠侧脑海马体中,48h后开展实验:A)潜伏期;B)第三象限时间;C)穿越平台次数;D)游泳轨迹;E)体内BACE1抑制活性;F)利用Western blot检测小鼠脑部APP-β,APP及DM1A表达水平;G)各组体内APP-β/APP分析值。该图显示,化合物1在体内对于AD病小鼠学习与记忆能力的影响,在对体内APP-β,APP及BACE1抑制活性的影响。与对照组相比较; ***p<0.001,**p<0.01,*p<0.05。
Figure.6.Cmp 1restored learning and memory impairments in 3xTg mice.1(2μg/μL×5μL,0.2μg/μL×5μL),LY2811376(2μg/μL×5μL)or vehicle was infused into the cerebroventricles of3xTg mice 48hours before starting the task.(A)Escape latencies to find the hidden platform were recorded daily.For the memory test,the time spent in the target quadrant was shown in(B),and the times of the platform crossing(C)and the swimming tracks(D)were calculated.(F)Western blot analyzed of protein levels of APP-βand APP and DM1A(G)Quantitative analysis.(E)BACE1activity in vivo was determined by beta-Secretase Activity Assay Kit.(H)The Aβ42levels in vivo were quantified through ELISA.Data were presented as means±sd.***p<0.001,**p<0.01,*p<0.05versus the vehicle control(n=10in each group).
图7:化合物1对于小鼠海马体中记忆相关蛋白的影响.A)采用Western blot检测synapsin-1,synaptophysin,psd 95及psd 93表达的影响;B)Western blot检测的定量分析;C)海马体CA3区显微图片;D)对神经纤维的影响。与对照组相比较;***p<0.001,**p<0.01,*p<0.05。该图显示了化合物1对于AD病小鼠脑内与记忆相关的关键蛋白表达及其对于神经纤维的影响,结果显示1能够明显增加相关蛋白的表达,且对于神经纤维的生长与发育具有一定的促进作用。
Figure 7.Cmp 1attenuated synaptic toxicity in hippocampus of 3xTg mice.(A)Western blot analysed of protein levels of synapsin-1,synaptophysin,psd 95and psd 93and(B)Quantitative analysis.(C)Representative photomicrographs of primary dendrites in the hippocampal CA3region.(D)Quantification of dendrite number and mushroom-type dendrites.Values were shown as mean±SD***p<0.001,**p<0.01,*p<0.05versus the vehicle group alone(n=10in each group).
图8:小鼠海马体尼氏染色图,A)尼氏染色典型照片;B)小鼠海马体CA3区细胞数目统计结果。尼氏染色主要反映化合物对于脑部神经的毒性作用,该图显示,化合物1对于海马体中神经细胞均无明显影响,提示化合物1无明显毒性。
Figure 8.Nissl staining of the cells numbers in hippocampus from compound 1(2μg/ul×5ul,0.2ug/ul×5ul),LY2811376(2μg/ul×5ul)and vehicle groups.A)Nissl staining(upper row,cells in hippocampus;lower row,cells in CA3.B)the quantification of cells in close bracket 3.The data were expressed as mean±SD,(n=3).
具体实施方式
实施例1:化合物土壤土曲霉菌素A和B的制备和结构鉴定。
(一)如式(1)所示土壤土曲霉菌素A,B和C
1.发酵条件
种子培养液的配置:取葡萄糖10.0g,麦芽膏3.0g,蛋白胨5.0g,酵母膏3.0g,溶于适量的水中,再以水定容至1000mL,123℃下高温灭菌40min,备用。将土壤来源土曲霉Aspergillus terreus QCX1-1接种到上述培养基中,100~120rpm,25~28℃条件下摇床培养为4天,得到种子培养液。
发酵:将200g大米置于1000mL锥形瓶中,加入200mL水后以123℃下高温灭菌40min,备用。将上述种子培养液接种到大米培养基中,25~28℃条件下静置培养28天。
2.提取分离
用工业酒精将发酵得到的菌丝体及培养基提取7次,低于50℃下减压浓缩回收工业酒精,得到1907.0g浸膏。将总浸膏100-200目硅胶拌样,并用干法装柱,以二氯甲烷-甲醇梯度洗脱(500:1–2:1),TLC检测,合并相同组分,共得到5个组分。组分3再经过反复的凝胶色谱、正反相硅胶柱色谱及高效液相色谱分离得到化合物土壤土曲霉菌素A(3.6mg),组分4经过反复的凝胶色谱、正反相硅胶柱色谱及高效液相色谱分离分到化合物土壤土曲霉菌素B(1.8mg)及土壤土曲霉菌素C(3.1mg)。
(二)如式(1)所示化合物土壤土曲霉菌素A,B和C结构鉴定
对化合物土壤土曲霉菌素A,B和C进行核磁共振,质谱,旋光,红外光谱,紫外光谱,圆二色谱等数据测试,对土壤土曲霉菌素A与C另进行X射线单晶衍射数据测试,对土壤土曲霉菌素B另进行ECD数据计算,从而确定化合物的结构。
土曲霉菌素A(化合物1):透明晶体, (浓度为0.9mg/mL,溶剂为 甲醇);UV(甲醇)λmax(logε)=249(3.99)与202(3.74)nm;NMR氢谱(400MHz)及碳谱(100MHz)如表1所示;高分辨质谱[M+Na]+m/z为451.2410(理论分子式及理论分子量分别为C26H36O5Na与451.2460)。化合物1绝对构型是通过X射线单晶衍射来确定的,晶体结构如图1所示,NMR数据如表1中所述。
土曲霉菌素B(化合物2):无色粉末, (浓度为1.5mg/mL,溶剂为甲醇);UV(甲醇)λmax(logε)=253(3.12)与209(3.31)nm;NMR氢谱(400MHz)与NMR碳谱(100MHz)如表1所示;高分辨质谱[M+Na]+m/z为499.2637(理论分子式及理论分子量分别为C26H36O5Na与499.2672)。土曲霉菌素B绝对构型的确定是通过生源途径比较来确定的,如图2所示,NMR数据如表1中所述。
土曲霉菌素C(化合物3):透明晶体, (浓度为2mg/mL,溶剂为甲醇);UV(甲醇)λmax(logε)=231(3.28)与202(3.81)nm;NMR氢谱(400MHz)与NMR碳谱(100MHz)如表1所示;高分辨质谱[M+Na]+m/z为 481.2199(理论分子式及理论分子量分别为C26H34O7Na与881.2202)。土曲霉菌素C的绝对构型是通过X射线单晶衍射来确定。晶体结构如图3所示,NMR数据如表1中所述。
表1.化合物1–3核磁谱(NMR)数据归属(溶剂为氯仿,氢谱400MHz,碳谱100MHz)
实施例2:化合物1-3抗阿尔茨海默病作用及对BACE1的抑制活性。
化合物1-3的抗阿尔茨海默病作用是先通过蛋白虚拟对接对8种与AD病密切相关的主要蛋白进行考察,其中发现上述化合物1和2最可能为BACE1抑制剂;利用荧光共振能量转移法(FRET法)对化合物1和2于细胞水平考察BACE1抑制活性;通过水迷宫法对3xTg小鼠水平进行抗阿尔茨海默病作用评价;并对其体内BACE1抑制活性,Aβ含量及其相关蛋白表达情况进行检测。结果如图4-8及表2,3所示:
实验结论:化合物1和2能够在体内及体外有效抑制BACE1活性,可以作为治疗抗阿尔茨海默病药物开发的先导化合物,其活性与阳性药一致。
表2化合物1和2与AD病相关蛋白虚拟对接分数(MF对接分数)a
a单位为(kcal/mol).
表3.化合物1–3体外抑制活性结果
a n.i.表示实验中对BACE1无抑制活性(IC50﹥40μM)。
土壤土曲霉次生代谢产物中抗阿尔茨海默病化合物及分离制备专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0