IPC分类号 : C07D491/22,C09K11/06,C12Q1/00,G01N21/64
专利摘要
本发明公开了结构式(I)所示的化合物,其中,R’为氢或C1~C18的烷基,R’’为C1~C18的烷基。本发明是一种可比率型检测G4 DNA的荧光探针,该探针通过共聚焦显微镜和超高分辨显微镜,成功实现了在活细胞或固定后细胞中对G4 DNA和溶酶体的同时检测,尤其是实现了重要癌靶标分子G4 DNA在活细胞中的原位、实时、超清晰成像。
权利要求
1.结构式(I)所示的化合物,
其中,R’为氢或C1~C18的烷基,R’’为C1~C18的烷基。
2.根据权利要求1所示的化合物,其特征在于:R’为氢或C1~C6的烷基,R’’为C1~C6的烷基。
3.权利要求1所示化合物的制备方法,其特征在于包括如下步骤:
化合物(A)与化合物(B)发生缩合反应得到结构式(I)所示的化合物,反应式如下:
4.根据权利要求3所述制备方法,其特征在于:反应温度为60~115 °C,使用醇、乙腈、芳香烃作为溶剂,在有机胺类催化下,通过缩合反应得到化合物(I)。
5.根据权利要求4所述制备方法,其特征在于:所述的醇选自甲醇、乙醇、异丙醇;芳香烃选自甲苯、苯;有机胺选自六氢吡啶、三乙胺、吡啶。
6.权利要求1所示化合物(I)在检测G-四链体 DNA中的应用。
7.权利要求1所示化合物(I)在细胞内同时检测溶酶体和G-四链体DNA的应用。
8.权利要求1所示化合物(I)在细胞荧光成像中的应用。
说明书
技术领域
本发明涉及螺吡喃类衍生物及在检测G-四链体 DNA和溶酶体中的应用,属于化学生物学传感器技术领域。
背景技术
长期以来,科学家们展开了大量针对癌症治疗的研究,旨在杀死、杀伤肿瘤细胞,同时又不影响正常细胞。近年来,随着癌症生物学的发展,越来越精确的靶向治疗方法被发现,其中,G-四链体(G4)DNA和溶酶体成为最新的精准抗癌靶标。
G4 DNA是一种非传统的核酸结构,是由富含串联重复鸟嘌呤(G)的DNA折叠形成的高级结构,已被证实可稳定存在于人体活细胞中(Biffi G, Tannahill D, McCafferty J,et al. Nature Chemistry, 2013, 5, 182)。它们不仅具有独特的结构,而且有着丰富的生物学功能。生物信息学表明,在人体基因组中大约含有~ 400000个可形成G4 DNA的序列,并位于基因组许多重要的生物学功能区域。但是这些序列在肿瘤抑制基因中很少,反而在促进肿瘤发生或增殖的原癌基因中比例很高,如一些重要的原癌基因的启动子区,包括C-myc、C-kit、KRAS、bcl-2和VEGF等基因序列中。2016年,剑桥大学的研究团队通过对癌变前的人类细胞系进行研究,检测到了差不多一万个G4。该项研究指出G4主要位于调控基因开关的DNA区域,特别是与癌症有关的基因,因此,G4 DNA现已成为癌症诊疗研究的新型靶标(Hänsel-Hertsch R, Beraldi D, Lensing S V, et al. Nature Genetics, 2016, 48,1267)。溶酶体一直以来都被误认为是细胞的“垃圾桶”,但我们现在知道这一结构更像是细胞的“胃”。通过溶酶体,大分子可由水解酶进行降解,这些酶包括各种负责蛋白降解的蛋白酶,降解后细胞也能获得相应的营养成分。而且溶酶体参与了多种细胞生命过程,如物质代谢、细胞膜循环、细胞凋亡以及信号转导等。在肿瘤细胞中的溶酶体体积比在正常细胞中更大。一项近期的研究表明,溶酶体也可作为理想的药物靶标,用于选择性摧毁癌细胞(Petersen N H T, Olsen O D, Groth-Pedersen L, et al. Cancer Cell, 2013, 24,379)。
将细胞中溶酶体和G4 DNA这两种靶标物可视化,不仅有助于理解溶酶体参与生命活动的分子机制, 而且对癌症的早期精准筛查具有重要的指导意义。近年来,分别靶向溶酶体和G4 DNA的分子光学探针已有报道,但目前为止,还受限于以下两点:1、未能实现比率型检测G4 DNA;2、未能实现在细胞中同时检测溶酶体和G4 DNA两种标靶物。
发明内容
本发明的目的是提供一种新型螺吡喃衍生物QIN及其制备方法。
本发明的另一个目的是将上述螺吡喃衍生物QIN作为荧光探针应用于G4 DNA的比率型检测,以及在细胞内对溶酶体和G4 DNA的同时检测和成像。
结构式(I)所示化合物,
其中,R’为氢或C1~C18的烷基,R’’为C1~C18的烷基;R’ 优选为氢或C1~C6的烷基,R’’优选为C1~C6的烷基。
上述化合物(I)的制备方法:化合物(A)与化合物(B)发生缩合反应得到化合物(I),反应式如下:
上述反应温度为60~115 °C,使用醇、乙腈、芳香烃作为溶剂,在有机胺类催化下,通过缩合反应得到化合物(I)。所述的醇选自甲醇、乙醇、异丙醇;芳香烃选自甲苯、苯;有机胺选自六氢吡啶、三乙胺、吡啶。
本发明化合物(I)可应用在检测G-四链体 DNA。
本发明化合物(I)可应用在细胞内同时检测溶酶体和G-四链体DNA。
本发明化合物(I)可应用在细胞荧光成像。
本发明在没有光或酸碱刺激下,G4 DNA也能够调控螺吡喃染料的开关和变色。G4DNA主要存在于细胞核内,而溶酶体作为细胞中的一种常见细胞器,位于细胞质区域,内含多种水解酶,其内环境的pH小于5.0,利用这种酸性环境的条件实现螺吡喃染料的变色。基于以上发现,本发明开发了可比率型检测G4 DNA的荧光探针化合物(I),并借助共聚焦显微镜和超高分辨显微镜,成功实现了这类分子在细胞(活细胞或固定后细胞)中对G4 DNA(核内)和溶酶体(核外)的同时比率型检测和成像。
本发明的优点:
(1)首次开发了可比率型检测G4 DNA的荧光探针,因为比率型检测不受底物和探针浓度、外部环境和仪器条件变化等影响,可有效避免检测时的背景干扰和假阳性,从而实现对G4 DNA和溶酶体的精准检测;
(2)该探针通过共聚焦显微镜和超高分辨显微镜,成功实现了在细胞(活细胞或固定后细胞)中对G4 DNA(核内)和溶酶体(核外)的同时检测,尤其是实现了重要癌靶标分子G4DNA在活细胞中的原位、实时、超清晰成像。
附图说明
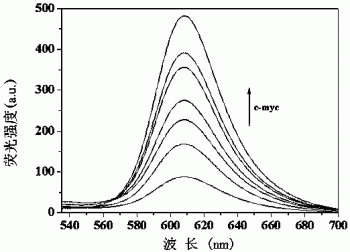
图1为荧光探针QIN-1在缓冲溶液中对C-myc G4 DNA不同浓度的荧光光谱;
图2为荧光探针QIN-1在缓冲溶液中对C-myc G4 DNA不同浓度的工作曲线图;
图3为荧光探针QIN-1在缓冲溶液中对G4 DNA、单链DNA、双链DNA的选择性柱状图;
图4为荧光探针QIN-1在缓冲溶液中对C-myc G4 DNA不同浓度的紫外光谱;
图5为荧光探针QIN-1在缓冲溶液中与C-myc G4 DNA圆二色谱;
图6为荧光探针QIN-1在活的正常细胞和癌细胞中的荧光成像图;
图7为荧光探针QIN-1在固定后HepG2细胞中DNA酶和RNA酶验证实验荧光成像图;
图8为荧光探针QIN-1在固定后U-2 OS细胞中DNA酶和RNA酶验证实验荧光成像图;
图9为荧光探针QIN-1在U-2 OS活细胞中的超分辨荧光成像图;
图10为荧光探针QIN-1在固定后U-2 OS细胞中DNA酶和RNA酶验证实验的超分辨荧光成像图。
具体实施方式
下面实施例中所使用的实验方法如无特殊说明,均为常规方法,所使用的材料、试剂等如无特殊说明,均可从商业途径得到。
实施例1荧光探针QIN-1的制备
在干燥的25 mL圆底烧瓶中,加入0.0717 g (0.33 mmol) 8-羟基久洛尼定-9-甲醛,0.0993 g (0.33 mmol) 1, 2, 3, 3-四甲基-3H-吲哚碘盐,30 μL哌啶和10 mL乙醇。回流9h。冷却,有粉红色固体析出,抽滤,乙醚洗涤滤饼,干燥得产物,即为荧光探针QIN-1,产量为0.0850g,产率为69%。
荧光探针QIN-1对C-myc G4 DNA不同浓度的荧光光谱测试:在5 mL的比色管中加入50μL 10
荧光探针QIN-1对C-myc G4 DNA不同浓度的工作曲线测定:由QIN-1对C-myc G4DNA不同浓度的荧光光谱得到在610 nm处荧光响应强度随C-myc G4 DNA浓度工作曲线图,如图2所示。由图2可知,当体系中逐渐加入C-myc G4 DNA 时,610 nm处的荧光强度与C-mycG4 DNA浓度呈现良好的线性关系,线性方程为y = 156.62 x + 96.066,相关系数为0.9913。
荧光探针QIN-1在G4 、单链DNA、双链DNA中选择性荧光光谱测试:在5 mL的比色管中加入50μL 10
荧光探针QIN-1对C-myc G4 DNA不同浓度的紫外光谱测试:在5 mL的比色管中加入50 μL 10
荧光探针QIN-1与C-myc G4 DNA的圆二色谱测试:配制总体积为400 μL的C-mycG4 DNA和QIN-1溶液,其中固定待测样品中C-myc G4 DNA的终浓度为5 μM,用QIN-1进行滴定测试,即QIN-1的浓度分别为0、5、10、15、20、25 μM,如图5所示。由图5可知,QIN-1在该条件下不改变G4 C-kit DNA的平行结构,当QIN-1的浓度逐渐增加时,265 nm处的峰越来越正,而240 nm处的峰越来越负。
荧光探针QIN-1细胞中G4 DNA和溶酶体荧光成像研究:分别在正常细胞MRC-5(人胚肺成纤维细胞)和HPASMC(人肺动脉平滑肌细胞),癌细胞HepG2(人肝癌细胞)、SMMC-7721(人肝癌细胞)、A375(人皮肤黑色素瘤细胞)、MCF-7(人乳腺癌细胞)、PC-3(人前列腺癌细胞)和U-2 OS(人骨肉瘤细胞)中加入75 nM的溶酶体标记物(LysoTracker Green DND-26)培养10 min,PBS清洗三次细胞后,加入100 µM的QIN-1,孵育10 min,PBS清洗三次细胞后,采用激光共聚焦拍摄荧光成像图片(激发波长为405 nm、488 nm和516 nm,收集435-485nm、500-545 nm、570-640 nm波长范围),得到荧光成像图6。向种有癌细胞HepG2和U-2 OS的三个培养皿中加入1 mL多聚甲醛,固定10 min,PBS清洗三次细胞后,分别加入QIN-1(100 µM)、QIN-1(100 µM)和DNA酶(100 units·mL
荧光探针QIN-1细胞中G4 DNA和溶酶体超分辨荧光成像研究:在种有U-2 OS细胞培养皿中,加入5 µg·mL
序列表
<110> 西北大学
<120> 螺吡喃类衍生物及在检测G-四链体 DNA和溶酶体中的应用
<160> 11
<170> SIPOSequenceListing 1.0
<210> 1
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
tgagggtggg tagggtgggt aa 22
<210> 2
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
agggagggcg ctgggaggag gg 22
<210> 3
<211> 23
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
gggcgcggga ggaagggggc ggg 23
<210> 4
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
agggttaggg ttagggttag gg 22
<210> 5
<211> 19
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
tggcctgggc gggactggg 19
<210> 6
<211> 15
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
aaaaaaaaaa aaaaa 15
<210> 7
<211> 15
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
tttttttttt ttttt 15
<210> 8
<211> 14
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
ggagggttgg gttt 14
<210> 9
<211> 14
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
aaacccaacc ctcc 14
<210> 10
<211> 30
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
aaaaaaaaaa aaaaattttt tttttttttt 30
<210> 11
<211> 28
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
ggagggttgg gtttaaaccc aaccctcc 28
螺吡喃类衍生物及在检测G-四链体DNA和溶酶体中的应用专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0