IPC分类号 : B01L3/00,C07K1/14,C07C229/36,C07C227/34,C07D498/06,C07B57/00
专利摘要
本发明公开了一种聚去甲肾上腺素功能化微流控芯片的制备方法及其在手性分离中的应用,属于微流控芯片技术领域。利用去甲肾上腺素在弱碱性条件下的自聚合反应,在微流控芯片通道内形成聚去甲肾上腺素涂层,极大改善了芯片通道的亲水性、生物相容性和电渗流稳定性,在聚去甲肾上腺素功能化微流控芯片上成功实现了苯丙氨酸对映体、氧氟沙星对映体以及二肽对映体的手性分离。
权利要求
1.聚去甲肾上腺素功能化微流控芯片的制备方法,其特征在于,称取去甲肾上腺素溶解于三羟甲基氨基甲烷盐酸盐缓冲溶液中,超声混匀,用微量注射器注入聚二甲基硅氧烷微流控芯片的缓冲池中,用真空泵将其抽入分离通道内,使去甲肾上腺素溶液布满整个分离通道,室温下静置反应完全,再用真空泵将超纯水抽入分离通道内,冲洗通道,即制备成聚去甲肾上腺素功能化的聚二甲基硅氧烷微流控芯片。
2.聚去甲肾上腺素功能化微流控芯片的手性分离应用,其特征在于:权利要求1所制备的聚去甲肾上腺素功能化的聚二甲基硅氧烷微流控芯片用于苯丙氨酸对映体、氧氟沙星对映体以及二肽对映体手性分离。
说明书
技术领域
本发明涉及一种聚去甲肾上腺素功能化微流控芯片的制备方法及其在手性分离中的应用,属于微流控芯片技术领域。
背景技术
手性是宇宙间的普遍特征,是自然界的本质属性之一。许多生理或药理化合物具有手性特性,它们在生物体内的生理活性和药理作用往往存在很大差别,其中一种对映体疗效高、毒副作用小,而另外一种对映体则一般不具有疗效或者药效弱,有的甚至抑制疗效且毒副作用强,以致对生命体产生不良反应。如,19世纪50年代,萨立多胺作为一种孕妇使用的镇定剂和安眠药而被熟知,然而服用了一段时间该药物的孕妇产下的婴儿均患有严重的海豹畸形。研究发现,萨立多胺是具有R型和S型2种光学异构体构型的手性药物,只有R-(+)-萨立多胺才能起到镇定剂和安眠的作用,而S-(-)-萨立多胺则具有致畸形的作用。除此之外,还有很多药物具有光学异构性,这些手性药物对映体之间的药效差别非常悬殊。惨痛的教训使人们深刻认识到,手性药物必须分别考察其异构体。因此,手性对映体拆分及组分鉴定在生物学和医药学领域具有重大而深远的意义。
自1858年LouisPasteur报道了首例对映体拆分以来,手性在生理系统中的作用引起了广泛关注,各种对映体拆分方法也应运而生。近年来,手性化合物的色谱和毛细管电泳分离方法发展迅速,成为手性分离的常用手段。微流控芯片电泳技术具有尺寸小、分析速度快、试剂消耗少、易实现多通道分离分析以及能够与其它操作单元进行整合等优点,成为手性分离以及不对称合成反应的理想平台。自从1999年Mathies等首次采用微流控芯片电泳技术实现了手性氨基酸的分离分析后,掀起了微流控芯片电泳技术分离手性物质的研究热潮。荧光标记技术、纳米技术、手性选择剂固定化技术以及芯片涂层技术等在微流控芯片电泳手性分离中的应用越来越广泛。常用的以聚二甲基硅氧烷(PDMS)芯片具有制作方便、快速且易于封合等优点,但其表面疏水性强、容易吸附被测物、电渗流不稳定,限制了PDMS芯片在手性物质分离方面的应用。采用合适的方法对芯片通道进行改性处理,可有效抑制非特异性吸附、提高分离效率及分离重现性。
去甲肾上腺素是一种类多巴胺的儿茶酚胺类小分子,在弱碱性条件下即可自聚合生成聚去甲肾上腺素(PNE)而粘附在几乎所有材料的表面。去甲肾上腺素的化学结构中,在儿茶酚基团旁边的脂肪碳原子上连接有羟基,使得PNE具有比聚多巴胺更稳定、形貌可控、生物相容性和亲水性更好的表面成膜性。因此,本发明发展了一种基于PNE功能化微流控芯片的制备方法并用于多种手性物质的分离。
发明内容
本发明的目的在于提供一种聚去甲肾上腺素功能化微流控芯片的制备方法,通过去甲肾上腺素自聚合作用在聚二甲基硅氧烷(PDMS)微流控芯片通道内形成涂层,进而应用于对多种手性物质的分离,它具有简单、绿色且分离效率高的特点。
本发明是这样实现的,在弱碱性条件下,去甲肾上腺素发生氧化聚合反应,在PDMS微流控芯片分离通道内形成具有良好亲水性和粘附性的PNE涂层,用于氨基酸对映体、药物对映体以及二肽对映体的分离。去甲肾上腺素在儿茶酚基团旁边的脂肪碳原子上连接有羟基,使得经PNE功能化的PDMS微流控芯片,不仅芯片通道的亲水性、生物相容性和电渗流稳定性得到了极大改善,而且,在整个修饰过程中,无需额外添加任何如有机溶剂等其它化学试剂,具有绿色环保、成本低廉、操作简单且快速等优点。测试结果表明,经PNE功能化的PDMS微流控芯片可成功用于对多种手性物质的分离分析。
本发明采用以下技术方案:
(1)聚去甲肾上腺素功能化微流控芯片的制备方法:称取10mg去甲肾上腺素溶解于2mL浓度50mMpH8.5的Tris-HCl缓冲溶液中超声混匀,用微量注射器注入聚二甲基硅氧烷(PDMS)微流控芯片的缓冲池中,用真空泵将其抽入分离通道内,连续抽10min使去甲肾上腺素溶液布满整个分离通道,室温下静置反应24h,再用真空泵将超纯水抽入分离通道内,连续抽5min冲洗通道,即制备成聚去甲肾上腺素(PNE)功能化的PDMS微流控芯片。
(2)聚去甲肾上腺素功能化微流控芯片的的手性分离应用:苯丙氨酸对映体、氧氟沙星对映体以及二肽对映体在聚去甲肾上腺素功能化PDMS微流控芯片上都实现了基线分离,分离度分别为1.5、2.5和2.8,表明聚去甲肾上腺素功能化PDMS微芯片对氨基酸对映体、药物对映体以及二肽对映体有良好的手性分离能力。
本发明的技术效果是:基于去甲肾上腺素在弱碱性条件下自聚合成膜特性的PDMS微流控芯片通道涂层,在PNE功能化PDMS微流控芯片上成功实现了苯丙氨酸对映体、氧氟沙星对映体以及二肽对映体的手性分离。在整个PNE涂层制备过程中,无需额外添加任何如有机溶剂等其它化学试剂,具有绿色环保、成本低廉、操作简单、快速,且能高效分离氨基酸对映体、药物对映体以及二肽对映体等优点。
附图说明
图1是NE自聚合过程的动态紫外光谱图。
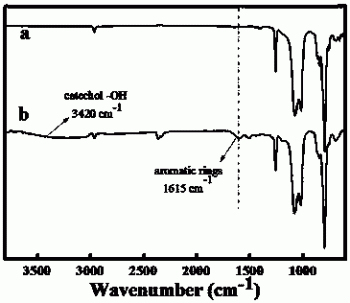
图2是(a)PDMS芯片和(b)PNE修饰PDMS芯片的傅里叶变换红外光谱图。
图3是(A)PDMS芯片和(B)PNE修饰PDMS芯片的接触角图。
图4是运行缓冲溶液pH对(a)PDMS芯片和(b)PNE修饰PDMS芯片EOF的影响。
图5是D-/L-苯丙氨酸在PNE修饰PDMS芯片上的分离条件优化:(A)检测电位,(B)分离电压,(C)NE聚合时间。
图6是(A)D-/L-苯丙氨酸,(B)外消旋氧氟沙星,(C)甘氨酸-D-/L-苯丙氨酸在(a)PDMS芯片和(b)PNE修饰PDMS芯片上的电泳分离图。
具体实施方式
下面结合附图和具体实施例对本发明作进一步阐述,本发明并不限于此;
实施例1
PDMS芯片的制作:以SU-8光刻胶(博奥生物有限公司)为模板,制作十字型PDMS微流控芯片通道。具体制作过程如下:将一定量的PDMS单体和固化剂按10:1(质量比)混合均匀、除气,倾注于SU-8模板上,在70oC固化2h。冷却后从模板上剥下含十字型通道的PDMS芯片,用刀片切割成所需形状,用打孔器在缓冲液池、样品池和样品废液池等三处打孔,形成直径为3mm的小孔。同时,以平滑玻璃板为模板,按照同样步骤制备不含微通道的PDMS盖片。将含十字通道的PDMS芯片和不含通道的PDMS盖片分别用二次水、甲醇、二次水超声清洗10min,在红外灯下烘干,随即将两片PDMS封合,形成一块可逆的PDMS芯片。PDMS分离通道长42mm(有效分离长度37mm),进样通道长10mm。所制得的PDMS分离通道呈梯形,上底宽50μm,下底宽65μm,深18μm。
实施例2
用真空泵将二次水充满整个PDMS芯片通道,称取10mg去甲肾上腺素溶解于2mL浓度50mMpH8.5的Tris-HCl缓冲溶液中超声混匀,用微量注射器注入PDMS烷微流控芯片的缓冲池中,用真空泵将其抽入分离通道内,连续抽10min使去甲肾上腺素溶液布满整个分离通道,室温下静置反应24h,再用真空泵将超纯水抽入分离通道内,连续抽5min冲洗通道,即制备成PNE功能化的PDMS微流控芯片。
图1是PNE的形成过程的动态紫外光谱表征。在50mMpH8.5的Tris-HCl缓冲溶液中,去甲肾上腺素(NE)逐渐发生氧化聚合。曲线a是NE溶液的紫外吸收光谱,在波长278nm处有NE的特征吸收峰,对应于NE结构中的儿茶酚基团。NE的氧化聚合随着时间的延长逐渐进行(曲线a-k),内插曲线a-k是从0h开始每隔1h测一个数据,波长为300-400nm的紫外光谱放大图。随着时间的延长,NE在278nm处的吸收峰逐渐消失,在342nm处产生了一个强度逐渐增加的新吸收峰,这是因为羰基连到苯环上时发生n-π*转换,对应于邻醌的特征吸收峰。UV-vis光谱的变化表明,在弱碱性条件下NE能够发生聚合形成PNE。
图2为PDMS芯片和PNE修饰PDMS芯片的傅里叶变换红外光谱图。与PDMS芯片(图2a)相比,PNE修饰PDMS芯片在1615cm-1和3420cm-1处分别出现了PNE的芳香环和儿茶酚的-OH特征吸收峰(图2b)。以上结果表明,PNE成功修饰于PDMS芯片通道表面。
图3是PDMS芯片和PNE修饰PDMS芯片的接触角表征图。PDMS芯片表面的非特异性吸附性主要由聚合物表面的疏水作用引起的。为了抑止PDMS芯片对生物分子的非特异性吸附,需对PDMS芯片表面进行改性,改善其亲水。由图3A可见,PDMS芯片的接触角为108°。而经PNE修饰后的PDMS芯片的接触角降低为13°(图3B),这是由于PNE中含有大量的氨基和儿茶酚羟基等亲水性基团所致。以上结果表明,通过PNE涂层修饰的PDMS芯片表面,其亲水性得到了极大改善,该芯片放置几周后接触角几乎不变,表明本修饰方法有良好的稳定性。
图4是PDMS芯片和PNE修饰PDMS芯片的电渗流随缓冲溶液pH(3-11)变化的关系曲线。在PDMS芯片上(图4a),电渗流(EOF)随pH的增加迅速增大,EOF难控制,稳定性较差,不利于电泳分离;而在PNE修饰PDMS芯片上(图4b),EOF随pH的增大变化较为平缓。此外,当pH为7.17时,PNE修饰PDMS芯片上EOF的相对标准偏差仅为0.53%(n=5),约为PDMS芯片的七分之一,表明在PNE修饰PDMS芯片上EOF的稳定性得到了有效改善。
实施例3
PNE功能化PDMS微流控芯片的应用:
(1)检测电位、分离电压和NE自聚合时间对电泳分离的影响
图5A为检测电位对电泳分离的影响,当检测电位低于+0.5V时,苯丙氨酸对映体的峰电流较小;随着检测电位的增加,对映体的峰电流逐渐增大;当检测电位高于+0.6V时,峰电流增加缓慢,继续增大检测电位导致背景电流随之增大,分析物难以达到基线分离。此外,当碳纤维工作电极承受过高电压时容易软化,为了延长工作电极的使用寿命以及考虑实验中检测信号的稳定性、重现性和信噪比,选择+0.6V(vs.Ag/AgCl)为检测电位。
图5B为在PNE修饰PDMS芯片上,D-/L-苯丙氨酸在不同分离电压下的电泳分离图。当分离电压从900V增加到1400V时,电泳峰逐渐变窄且更加对称,迁移时间逐渐缩短。当分离电位超过1200V时,产生的焦耳热使得基线不稳定,D-/L-苯丙氨酸的分离度和分离效率下降。综合考虑分离效率、分析时间、灵敏度和信噪比,选择1200V为分离电位。
图5C为NE聚合时间对电泳分离的影响,当聚合时间低于24h时,随着时间的延长,PNE层在通道表面逐渐形成,通道的亲水性和电渗流稳定性得到改善,D-/L-苯丙氨酸的分离度不断增大。当聚合时间大于24h时,分离度增加缓慢。因此,选择聚合时间为24h。
(2)图6为D-/L-苯丙氨酸、R-/S-氧氟沙星、甘氨酸-D-/L-苯丙氨酸在PDMS芯片和PNE修饰PDMS芯片上的分离电泳图。在PDMS芯片上,三种对映体均无法实现基线分离;而在PNE修饰PDMS芯片上,D-/L-苯丙氨酸、R-/S-氧氟沙星、甘氨酸-D-/L-苯丙氨酸均在100s以内达到良好的基线分离,分离度分别为1.5、2.5、2.8。理论塔板数分别为D-/L-苯丙氨酸1.3×104plates/m和1.04×104plates/m,R-/S-氧氟沙星1.37×104plates/m和1.15×104plates/m,甘氨酸-D-/L-苯丙氨酸4.6×104plates/m和6.5×104plates/m。以上结果表明,本发明方法制备的PNE功能化PDMS微流控芯片对氨基酸对映体、药物对映体以及二肽对映体具有良好的分离功能。
聚去甲肾上腺素功能化微流控芯片的制备方法及其手性分离应用专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0