专利摘要
本发明涉及基于极窄带半导体为固体导电通道的光催化剂及其制备方法和应用。通过溶胶水热和煅烧方法制备,在Er3+:Y3Al5O12@NiGa2O4和Bi2Sn2O7之间插入一个极窄带隙半导体CoS2,形成了一个新型的Z型光催化体系。制备的光催化剂的光催化活性通过在模拟太阳光照射下对亚硝酸盐和亚硫酸盐的转化来评估。结果表明,所制备的Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7复合材料在亚硝酸盐和亚硫酸盐转化过程中表现出了高度稳定的光催化活性。
权利要求
1.基于极窄带半导体为固体导电通道的光催化剂,其特征在于:所述的基于极窄带半导体为固体导电通道的光催化剂是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。
2.权利要求1所述的基于极窄带半导体为固体导电通道的光催化剂的制备方法,其特征在于,包括如下步骤:将适量Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末和Bi2Sn2O7纳米粉末加入到无水乙醇中,超声分散,所得悬浮液加热煮沸,于100℃下恒温30-40min,过滤干燥,所得粉末研细,在马弗炉中,200℃煅烧2.0h后取出,研磨,得到Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。
3.如权利要求2所述的制备方法,其特征在于:所述的Er3+:Y3Al5O12@NiGa2O4/CoS2制备方法为:于Er3+:Y3Al5O12@NiGa2O4纳米粉末中加入适量无水乙醇,超声分散,在40-60℃下,用磁力搅拌器混合均匀,搅拌半小时后加入CoS2粉末,然后用无水乙醇和蒸馏水清洗,离心干燥后,放入马弗炉中,在500℃焙烧2h后取出,研磨,得到Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末。
4.如权利要求3所述的制备方法,其特征在于:所述的Er3+:Y3Al5O12@NiGa2O4纳米粉末的制备方法包括如下步骤:将Ga2O3固体加入到硝酸镍溶液中,产生的混合液调节pH到12,然后加入Er3+:Y3Al5O12继续搅拌20min,得到的悬浮溶液转移到反应釜中,180℃下反应48h,冷却至室温,得到沉淀物用去离子水清洗,然后在80℃下烘干8h,得到Er3+:Y3Al5O12@NiGa2O4粉体,将粉体研细,在500℃的马弗炉中,焙烧2h,取出后再经研磨,即得到Er3+:Y3Al5O12@NiGa2O4纳米粉末。
5.如权利要求3所述的制备方法,其特征在于:所述的CoS2制备方法为:将适量CoCl2和Na2S2O3溶解在去离子水中,超声30分钟,得到的悬浮溶液转移到反应釜中,200℃下反应16h,冷却至室温,得到沉淀物用去离子水清洗,然后在60℃下烘干8小时,得到CoS2粉末。
6.如权利要求2所述的制备方法,其特征在于:所述的Bi2Sn2O7制备方法为:将适量Bi(NO3)3·5H2O和K2SnO3·3H2O混合于去离子水中,边搅拌边调节PH=12,超声30分钟,得到的悬浮溶液转移到反应釜中,180℃下反应24h,冷却至室温,得到沉淀物用去离子水清洗,然后在60℃下烘干8小时,得到Bi2Sn2O7粉体。
7.权利要求1所述的基于极窄带半导体为固体导电通道的光催化剂在光催化转化亚硝酸盐和亚硫酸盐中的应用。
8.如权利要求7所述的应用,其特征在于,方法如下:于含有亚硝酸盐和亚硫酸盐的水溶液中,用500W氙灯照射,光照时间为4.0h。
说明书
技术领域
本发明属于光催化领域,具体的涉及一种基于极窄带半导体为固体导电通道的光催化剂 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的制备方法及在光催化转化亚硝酸盐和亚硫酸盐中的应用。
背景技术
水是人类生活和生产活动不可缺少的。在现代生活中,由于工业废水和生活污水流入河流和湖泊,水污染严重。水污染直接危害人类健康,对社会生活造成巨大的负面影响。其中,地表水和地下水的亚硝酸盐和亚硫酸盐污染已经非常严重。这种紧迫的污染危机已经引起了全世界的关注。亚硝酸盐可作为食品着色剂和防腐剂,主要来自食品工业废水。含有高浓度亚硝酸盐的地下水会导致人体出现高铁血红蛋白血症,导致智力低下甚至死亡。亚硫酸盐主要来自造纸,制革,制药,人造纤维,电镀工业废水排放的废水。不仅影响水质,而且随着酸度的增加,还会产生二氧化硫,进一步污染环境。亚硝酸盐和亚硫酸盐含量过高会破坏水生动物的免疫系统,诱发各种疾病。研究亚硝酸盐和亚硫酸盐的处理对于保护和改善环境具有重要的现实意义。因此,必须尽可能减少水中亚硝酸盐和亚硫酸盐的含量。各种处理方法已被开发用于处理亚硝酸盐和亚硫酸盐,如电子透析,反渗透,离子膜,生物降解和光催化技术等。在所有的方法中,光催化被认为是一种可行的和有前途的水污染处理技术。
Z型光催化体系经适当改性后可以同时具有较强的氧化性和较强的还原性。两个合适的带隙半导体的组合和适当的电子通道的引入可以控制光生电子空穴对的复合并且扩大光的响应范围,非常适合亚硝酸盐和亚硫酸盐的太阳光光催化转化。选择合适的带隙结构的半导体光催化剂具有重要意义。NiGa2O4具有较宽的3.54eV带隙,可以吸收高能量的太阳光,并且由于较负的导带而具有更强的还原性。Bi2Sn2O7具有2.79eV的窄带隙,可以吸收低能量的太阳光,并且由于更正的价带而具有强氧化性。在NiGa2O4/Bi2Sn2O7光催化体系中,可以看出,NiGa2O4的价带与Bi2Sn2O7的导带较为接近。此外,NiGa2O4作为宽带隙半导体,仅在紫外光照射(λ≤350nm)下才能激发,并且紫外光仅占太阳光的一小部分。这限制了NiGa2O4在亚硝酸盐和亚硫酸盐光催化转化中的应用。
发明内容
为了加快电子转移速率,本发明设计合成一种将极窄带半导体CoS2作为导电通道来有效分离光生电子和空穴的新型复合光催化剂Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。本发明所涉及化合物属于新型Z型半导体光催化剂,将其应用于同时转化亚硝酸盐和亚硫酸盐并生成硫酸铵化肥中,操作简单、无污染、催化剂稳定性好、易于分离。
本发明采用的技术方案是:基于极窄带半导体为固体导电通道的光催化剂,所述的基于极窄带半导体为固体导电通道的光催化剂是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。
上述的基于极窄带半导体为固体导电通道的光催化剂的制备方法,包括如下步骤:将适量Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末和Bi2Sn2O7纳米粉末加入到无水乙醇中,超声分散,所得悬浮液加热煮沸,于100℃下恒温30-40min,过滤干燥,所得粉末研细,在马弗炉中,200℃煅烧2.0h后取出,研磨,得到Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。
上述的制备方法,所述的Er3+:Y3Al5O12@NiGa2O4/CoS2制备方法为:于 Er3+:Y3Al5O12@NiGa2O4纳米粉末中加入适量无水乙醇,超声分散,在40-60℃下,用磁力搅拌器混合均匀,搅拌半小时后加入CoS2粉末,然后用无水乙醇和蒸馏水清洗,离心干燥后,放入马弗炉中,在500℃焙烧2h后取出,研磨,得到Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末。
上述的制备方法,所述的Er3+:Y3Al5O12@NiGa2O4纳米粉末的制备方法包括如下步骤:将Ga2O3固体加入到硝酸镍溶液中,产生的混合液调节pH到12,然后加入Er3+:Y3Al5O12继续搅拌20min,得到的悬浮溶液转移到反应釜中,180℃下反应48h,冷却至室温,得到沉淀物用去离子水清洗,然后在80℃下烘干8h,得到Er3+:Y3Al5O12@NiGa2O4粉体,将粉体研细,在500℃的马弗炉中,焙烧2h,取出后再经研磨,即得到Er3+:Y3Al5O12@NiGa2O4纳米粉末。
上述的制备方法,所述的CoS2制备方法为:将适量CoCl2和Na2S2O3溶解在去离子水中,超声30分钟,得到的悬浮溶液转移到反应釜中,200℃下反应16h,冷却至室温,得到沉淀物用去离子水清洗,然后在60℃下烘干8小时,得到CoS2粉末。
上述的制备方法,所述的Bi2Sn2O7制备方法为:将适量Bi(NO3)3·5H2O和K2SnO3·3H2O 混合在去离子水中,边搅拌边调节PH=12,超声30分钟,以促进其反应完全。得到的悬浮溶液转移到反应釜中,180℃下反应24h,冷却至室温,得到沉淀物用去离子水清洗,然后在60℃下烘干8小时,得到Bi2Sn2O7粉体。
上述的基于极窄带半导体为固体导电通道的光催化剂在光催化转化亚硝酸盐和亚硫酸盐中的应用。方法如下:于含有亚硝酸盐和亚硫酸盐的水溶液中,用500W氙灯照射,光照时间为4.0h。
上述基于极窄带半导体为固体导电通道的光催化剂 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7在模拟太阳光照射下,转化亚硝酸盐和亚硫酸盐的过程分析:由于NiGa2O4价带与Bi2Sn2O7导带电位相近,Bi2Sn2O7导带电子容易转移到 NiGa2O4价带空穴上。但是为了进一步提高他们的转移速率。本发明选择了将带宽更窄的 CoS2作为固体导电通道。NiGa2O4价带上的电子具有很强的还原能力,它能够使具有一定氧化性的NO2-还原,分别生成了NH4+和N2。具体的产物取决于pH,pH小于7的酸性条件容易生成NH4+离子,pH值大于7的碱性条件容易生成N2。同时在Bi2Sn2O7的价带上SO32-被价带上的空穴氧化为SO42-,能够与生成的NH4+结合生成硫酸铵((NH4)2SO4)。实际上在NO2-和SO32-处理过程中,最终生成含有硫酸铵((NH4)2SO4)的水溶液,经过适当处理可以作为化肥直接使用。
本发明的有益效果:
本发明制备的Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化剂性质稳定,耐高温,耐酸碱腐蚀,与单纯的Er3+:Y3Al5O12@NiGa2O4和Bi2Sn2O7相比,本发明的催化剂在太阳光的照射下转化亚硝酸盐和亚硫酸盐的效率有了大幅度提高。本发明中复合光催化剂 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7不仅具有传统光催化剂的优点,而且其最值得关注的是针对NiGa2O4和Bi2Sn2O7带宽特点以及导带和价带位置独特性,设计了一种将CoS2作为导电通道的新型光催化剂。该方法解决了光生电子和空穴复合的问题,大幅度的提高了光催化转化亚硝酸盐和亚硫酸盐的效率。
附图说明
图1是NiGa2O4,Bi2Sn2O7和Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的光致发光光谱(PL) 图。
图2a是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的X射线光电子能谱(XPS)图。
图2b是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Er元素的XPS图。
图2c是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Y元素的XPS图。
图2d是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Al元素的XPS图。
图2e是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Ni元素的XPS图。
图2f是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Ga元素的XPS图。
图2g是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Bi元素的XPS图。
图2h是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Sn元素的XPS图。
图2i是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的S元素的XPS图。
图2j是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的O元素的XPS图。
图2k是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的Co元素的XPS图。
图3是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的透射电子显微镜(TEM)图。
图4是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的红外光谱(IR)图。
图5a是模拟太阳光照射时间对亚硝酸盐和亚硫酸盐的光催化转化率的影响图。
图5b是相应的反应动力学对亚硝酸盐和亚硫酸盐的光催化转化率的影响图。
图6a是制备样品的光催化活性对亚硝酸盐和亚硫酸盐的光催化转化率的影响图。
图6b是使用次数对亚硝酸盐和亚硫酸盐的光催化转化率的影响图。
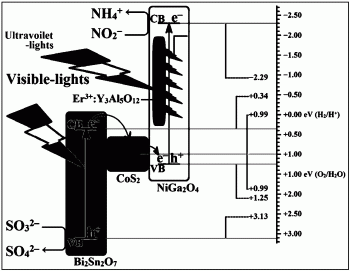
图7是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化转化亚硝酸盐和亚硫酸盐机理。
具体实施方式
实施例1Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7
(一)制备NiGa2O4纳米粉末
将0.376g Ga2O3粉末加入到50mL 1mol/L硝酸镍溶液中,产生的混合物用氢氧化钠调节pH到12(边调边搅拌30min),得到的悬浮溶液转移到反应釜中180℃下反应48h,冷却至室温,得到浅蓝色沉淀物用去离子水清洗数遍,然后在60℃下烘干8h,得到NiGa2O4粉体。将粉体研细,在500℃的马弗炉中,焙烧2h,取出后再经研磨,即得到NiGa2O4纳米粉末。
(二)制备CoS2纳米粉末
将2.62g CoCl2和3.16g Na2S2O3溶解在60ml去离子水中,超声30分钟,得到的悬浮溶液转移到反应釜中,200℃下反应16h,冷却至室温,得到沉淀物用去离子水清洗数遍,然后在60℃下烘干8小时,得到CoS2粉体。
(三)制备Bi2Sn2O7纳米粉末
将8.76g Bi(NO3)3·5H2O和5.40g K2SnO3·3H2O混合在150ml去离子水中,边搅拌边用氨水或氢氧化钾调到PH=12。超声30分钟,以促进其反应完全,得到的悬浮溶液转移到反应釜中,180℃下反应24h,冷却至室温,得到沉淀物用去离子水清洗数遍,在60℃下烘干8小时,得到Bi2Sn2O7粉体。
(四)制备Er3+:Y3Al5O12纳米粉末
将0.032g Er2O3(99.99%)、5.679g Y2O3(99.99%)粉末溶解在100mL浓硝酸(65.00%)中并磁力加热搅拌直至无色透明。然后按比例称取Al(NO3)3·9H2O(99.99%)溶解在蒸馏水中,在室温下用玻璃棒搅拌并慢慢加入到稀土离子溶液中。将柠檬酸作为螯合剂和助溶剂,按照n 柠檬酸:n稀土离子=3:1称取柠檬酸,并用蒸馏水溶解,在50-60℃加热搅拌,当溶液呈粘稠状时停止。在这个过程中没有沉淀生成,最终得到发泡黏胶状溶液。将粘稠状溶液放入烘箱恒温80℃加热36h。在干燥过程中直到蒸干溶剂没有沉淀物生成,最终得到泡沫溶胶。得到的溶胶在500℃加热50min,然后分别在1100℃分别煅烧2h。最后,从高温炉中取出烧结的物质并且在空气中冷却至室温得到Er3+:Y3Al5O12粉末。
(五)制备Er3+:Y3Al5O12@NiGa2O4纳米粉末
将0.376g Ga2O3固体加入到50mL 1mol/L硝酸镍溶液中,产生的混合液用1mol/L氢氧化钠调节pH到12(边调边搅拌30min),然后加入Er3+:Y3Al5O12继续搅拌20min。得到的悬浮溶液转移到反应釜中,180℃下反应48h,冷却至室温,得到沉淀物用去离子水清洗数遍,然后在80℃下烘干8h,得到Er3+:Y3Al5O12@NiGa2O4粉体。将粉体研细,在500℃的马弗炉中,焙烧2h,取出后再经研磨,即得到Er3+:Y3Al5O12@NiGa2O4纳米粒子。
(六)制备Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末
将6g Er3+:Y3Al5O12@NiGa2O4粉末放入烧杯中加入200mL无水乙醇,超声分散30min,在40~60℃下,用磁力搅拌器混合均匀,搅拌半小时后加入CoS2粉末,然后用无水乙醇和蒸馏水清洗数次,离心干燥后,放入马弗炉中在500℃焙烧2h后取出,研磨,得到 Er3+:Y3Al5O12@NiGa2O4/CoS2纳米粉末。
(七)制备Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7纳米粉末
将6g Er3+:Y3Al5O12@NiGa2O4/CoS2和6g Bi2Sn2O7纳米粉末加入到200mL无水乙醇中,超声分散30min,将悬浮液加热煮沸恒温30min,过滤后于60℃下干燥8.0h,将粉末研细,在马弗炉中,200℃煅烧2.0h后取出,研磨,得到 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7。
(八)检测
(1)图1是NiGa2O4,Bi2Sn2O7和Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的光致发光光谱(PL) 图片分析。
光致发光(PL)光谱是确定半导体中光生电子空穴对复合的重要方法。一般来说,PL 光谱中较低强度的信号表明电子空穴对的复合速率较低。相反,较高的强度显示较高的电子空穴对复合率。从图1中可以清楚地看出Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的PL强度比Er3+:Y3Al5O12@NiGa2O4和Bi2Sn2O7低,说明Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7具有较低的电子空穴对复合速率。(1)NiGa2O4和Bi2Sn2O7形成Z型光催化体系,Bi2Sn2O7的导带上的光生电子可以与NiGa2O4的价带上的光生空穴重新结合。(2)CoS2的导带和价带的位置位于Bi2Sn2O7的导带位置和NiGa2O4的价带之间。由于窄带半导体的存在,成为加速电子传输速率的导电通道。
(2)图2a-图2k是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的X射线光电子能谱(XPS)图片分析。
用X射线光电子能谱(XPS)研究了Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的化学组成。从图2a-图2k可以看出,Er,Y,Al,O,Ni,Ga,S,Bi,Co和Sn元素的峰可以被发现。在74.0eV(Al 2p),157.4eV(Y 3d),173.7eV(Er 4d)和530.5(O 1s)处出现的峰与Er3+:Y3Al5O12的组成相一致。在530.5eV(O 1s)和20.5eV(Ga 3d)处呈现的峰与NiGa2O4的组成紧密相符。Bi2Sn2O7的Bi(4f7/2)和Bi(4f5/2)峰分别为158.7和164.5eV,说明Bi2Sn2O7中存在Bi3+。 Sn(3d5/2)和Sn(3d3/2)在486.9和494.8eV处出现两个峰,说明存在Sn4+。这些结果表明预测的Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7已被制备。
(3)图3是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的透射电子显微镜(TEM)图片分析。
通过图3所示的透射电子显微镜(TEM)进一步进行深入观察。从图3(a-1)可以确定尺寸较大的规则颗粒是Er3+:Y3Al5O12@NiGa2O4颗粒。Er3+:Y3Al5O12@NiGa2O4中较暗的部分是Er3+:Y3Al5O12,其被包裹NiGa2O4中。可以看出,尺寸为20-50nm的较小颗粒被确定为 Bi2Sn2O7颗粒。另外,在Er3+:Y3Al5O12@NiGa2O4和Bi2Sn2O7之间,还有许多更小的粒子,这应该是CoS2纳米粒子。图3(a-2)中进一步放大的TEM可以看出它们的确切关系和组成。在图3(a-2)中,0.298,0.281,0.331和0.314nm的测量点分别与Er3+:Y3Al5O12的d221平面, NiGa2O4的d220平面,Bi2Sn2O7的d311平面和CoS2的d111平面相匹配。通过TEM研究,不仅可以确定其结构和组成,而且可以证明预测的Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7已经被制备了。
(4)图4是Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的红外光谱(IR)图片分析。
为了提供关于制备样品结构的化学信息,测定了制备的 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的红外光谱,相应的结果如图4所示。图4中,在 3430cm-1处的峰是由于ν(OH)伸缩振动得到的。在约789cm-1处的金属氧振动是Y-O伸缩频率的特征,这可能是Er3+:Y3Al5O12。在图4中,红外光谱清楚地显示了两个强吸收峰的存在。在455cm-1处的吸收峰归属于四面体位点中金属氧的伸缩振动模型,约692cm-1处的峰属于八面体配合物。根据这两个吸收峰可以确认,形成了具有亚晶格四面体部位和八面体部位的单相尖晶石结构的NiGa2O4。在515cm-1和634cm-1处的峰分别归因于BiO8十二面体中的Bi-O伸缩振动和Bi2Sn2O7的SnO6八面体中的Sn-O伸缩振动。在图4中,出现在1116 cm-1的峰归属于CoS2的Co=O弯曲振动模式。
实施例2Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7在光催化转化亚硝酸盐和亚硫酸盐中的应用
(一)模拟太阳光照射时间和相应的反应动力学对亚硝酸盐和亚硫酸盐的光催化转化率的影响
在模拟太阳光照射下进行Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化剂对亚硝酸盐和亚硫酸盐的光催化转化。在光照射之前,将含有NO2-和SO32-的溶液在黑暗中搅拌30分钟,并达到吸附-解吸平衡。然后,每1.0小时取出溶液样品,通过离子色谱法检测亚硝酸盐和亚硫酸盐的转化率。从图5a-1可以看出,随着模拟太阳光照射时间的增加,光催化转化率呈上升趋势。在太阳光4.00小时照射下,对于NO2-和SO32-,其光催化转化率分别可达82.32%和92.18%,NH4+,NO3-,N2和SO42-生成率分别为70.83%,10.17%,1.32%和90.89%。从实验结果可以看出,NO3-和N2的生成率远远低于NH4+,这表明在设计的Z型 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化体系中,在pH=5.00时大部分NO2-转化为NH4+。此外,在图5a-1中,SO32-的转化率略低于SO42-的产率,这可能是由于SO32-可以转化除SO42-之外的少量其他含硫化合物。
为了推测亚硝酸盐和亚硫酸盐的模拟太阳光光催化转化反应式,如图5a-2所示,对反应动力学进行了研究。可以看出,一阶反应和照射时间(t)的所有-ln(Ct/C0)(Ct:t照射时间的瞬时浓度,C0:初始浓度)数据可以认为大致呈现线性关系。对应于NO2-和SO32-的反应动力学方程分别为-ln(Ct/C0)=0.4502t+0.0137(R2=0.9870)和-ln(Ct/C0)=0.6739t-0.0879(R2= 0.9681)。对于NO2-和SO32-,比率常数分别为0.4502min–1,0.6739min–1。
(二)比较制备样品的光催化活性和使用次数对亚硝酸盐和亚硫酸盐的光催化转化率的影响
模拟太阳光照射下进行了在三种制备的光催化剂(Er3+:Y3Al5O12@NiGa2O4,Bi2Sn2O7和 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7)存在下亚硝酸盐和亚硫酸盐的光催化转化。从图6a 可以看出,三种制备的光催化剂存在时水溶液中的亚硝酸盐和亚硫酸盐转化率不同,其转化率取决于所用的光催化剂。对于NiGa2O4来说,作为宽带隙半导体光催化剂,它具有更负的导带(CB),显示出更强的还原性。NO2-可以转化为NH4+和N2,在模拟太阳光照射下,NiGa2O4的导带(CB)上,NO2-的转化率较高并且NH4+的生产率也较高。对于Bi2Sn2O7,作为窄带隙半导体光催化剂,它具有更有效的价带(VB),显示更强的氧化性,SO32-可转化为 SO42-,并且可以在价带上获得较高的转化率。Z型光催化剂 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7同时具有更负的导带(CB)和更正的价带(VB)。显然,在模拟太阳光的照射下,NO2-和SO32-的转化率高于单一的光催化剂Er3+:Y3Al5O12@NiGa2O4或Bi2Sn2O7的转化率。另外,由于CoS2用作导电通道,进一步提高了电子转移速率。
通过进行亚硝酸盐和亚硫酸盐在模拟太阳光下光催化转化重复实验,评估了 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7的稳定性,如图6b所示。显然,对于 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7,随着使用次数的增加,亚硝酸盐和亚硫酸盐的模拟太阳光光催化转化率略有下降。在模拟太阳光照射下经过五次重复使用后NO2-和SO32-的转化率分别达到74.23%和85.38%。表明在模拟太阳光照射下 Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化剂可以长时间保持较高的性能。
Er3+:Y3Al5O12@NiGa2O4/CoS2/Bi2Sn2O7光催化转化亚硝酸盐和亚硫酸盐机理:为了有效地抑制导带上的电子和价带上的空穴的复合,将NiGa2O4和Bi2Sn2O7组合以形成Z型光催化体系是必要的。然而,电子流速较慢会降低Z型光催化体系的活性。最近有报道贵金属被用作导电通道来加速电子流速。尽管如此,在实际应用中还是有一些显着的缺陷。所使用的贵金属具有窄且固定的能级,其可能偏离Bi2Sn2O7导带和NiGa2O4的价带,这不利于光生电子通过贵金属的流动。另外,使用贵金属还会增加光生电子的运行距离。
为了避免贵金属作为导电通道带来的问题,可以选择非常窄的带隙半导体CoS2作为固体导电通道来加速电子传输速率。窄带半导体导带位置非常接近Bi2Sn2O7的导带位置,窄带半导体的价带位置非常接近于NiGa2O4价带位置。由于窄带半导体的加入与Bi2Sn2O7和NiGa2O4结合,形成一系列差异较小的电子能级。通过窄带半导体作为导电通道,Bi2Sn2O7导带上的光生电子很容易转移到NiGa2O4价带上。而且,CoS2作为无机材料的窄带半导体,与NiGa2O4和Bi2Sn2O7具有一定的相容性。它们相互结合良好,形成较大的接触面积。由窄带半导体形成的导电通道的电阻很小,这有利于加速电子的传输速率。
基于极窄带半导体为固体导电通道的光催化剂及其制备方法和应用专利购买费用说明

Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
![]()
动态评分
0.0